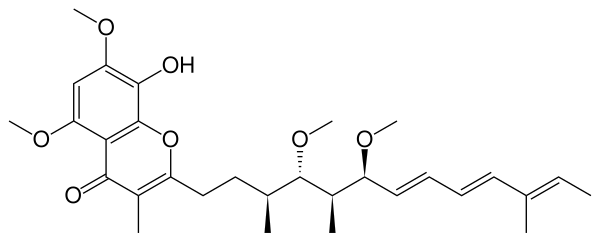
Стигмателлин
Стигмателлин — мощный ингибитор сайта окисления хинола (Qout-сайта) цитохром-bc1-комплекса митохондрий и цитохром-b6f-комплекса в мембране тилакоидов.
Стигмателлин был выделен из миксобактерии Stigmatella aurantica и содержит 5,7-диметокси-8-гидроксихромоновую ароматическую группу с алкеновой цепью во втором положении. Были получены структуры bc1-комплексов быка и дрожжей (Saccharomyces cerevisiae), ингибированных стигмателлином. Он связывается в Qout-сайте цитохрома b, дистальнее гема bL и взаимодействует с остатком гистидина (His-181) белка Риске при помощи водородной связи. Этот остаток гистидина служит лигандом железосерного кластера [2Fe-2S]. Водородная связь повышает редокс-потенциал железосерного кластера с 290 до 540 мВ и сковывает движения цитоплазматического домена Белка риске[1].
Общие сведения
| Стигмателлин | |
|---|---|
| Общие | |
| Хим. формула | C30H42O7 |
| Физические свойства | |
| Молярная масса | 514,65 г/моль |
| Классификация | |
| Рег. номер CAS | 91682-96-1 |
| 3D model (JSmol) | Интерактивная схема |
| PubChem | 447884 |
| CompTox Dashboard EPA | DTXSID40903940 |
| Рег. номер EINECS | 620-944-2 |
| SMILES | |
| InChI | |
| ChEBI | 32155 |
| ChemSpider | 394850 |
| ECHA InfoCard | 100.149.842 |
Примечания
Литература
- von Jagow, G., and Link, T.A. Methods in Enzymology 126: 253—271 (1986)