Смесь (химия)
Сме́сь — система, состоящая из двух или более веществ (компонентов смеси). Гомогенную (однородную)смесь называют раствором (газовым, жидким или твёрдым), а гетерогенную (неоднородная) — механической смесью[1]. Гомогенная система в каждой точке объёма имеет одинаковый состав, граница раздела фаз отсутсвует, например: природный газ, раствор поваренной соли в воде, нефть, сталь, чугун и др. В гетерогенной смеси вещества находятся в разных фазах, например: смесь воды и масла, дым и др.
Смесь можно разделить на компоненты физическими методами; изменения состава компонентов смеси при этом не происходит[2]. В результате разделения смесей происходит выделение компонентов в чистом виде. Способы разделения основаны на различии в физических свойствах компонентов.
Составляющие вещества, индивидуальные вещества, чистые вещества и смеси
Традиционная эмпирическая классификация веществ в химии основана на их делимости на составные части и не использует представлений атомно-молекулярной теории[1]. В отечественной литературе принято делить химические вещества на индивидуальные (чистые) вещества (простые и соединения) и их смеси[3][4]. На сегодняшний день стандартизированное определение индивидуального вещества отсутствует, поэтому в физической химии в качестве его синонима используют термин составляющее вещество[5], понимая под ним любое вещество, которое может быть выделено из системы и существовать вне её[6] (иногда говорят не о составляющих веществах и независимых составляющих веществах — компонентах, — а о компонентах и независимых компонентах)[7][8]. Отказ от использования терминов «чистое вещество» и «индивидуальное вещество» исключает произвол, связанный с привязкой этих понятий к степени чистоты вещества и требованиям постоянства его состава и свойств.
Классификация смесей
В зависимости от фазового состава различают[9]:
- гомогенную смесь, представляющую собой однородную систему, химический состав и физические свойства которой во всех частях одинаковы или меняются непрерывно, без скачков (между частями системы нет поверхностей раздела). Составные части гомогенной смеси нельзя отделить друг от друга механическими методами;
- гетерогенную смесь, состоящую из однородных частей (фаз), разделённых поверхностью раздела. Фазы могут отличаться друг от друга по составу и свойствам. Составные части гетерогенной смеси можно отделить друг от друга механическими методами. К гетерогенным смесям относятся, например, композиты.
Гомогенные смеси делят по агрегатному состоянию на три группы[4]:
- газовые смеси (газовые растворы), например, атмосферный воздух;
- растворы (жидкие растворы), например, раствор сахара в воде, природная вода, нефть и нефтепродукты;
- твёрдые растворы, например, природный минерал электрум и входящий в состав углеродистых сталей аустенит.
В зависимости от агрегатного состояния компонентов в гетерогенных смесях различают[10]:
| Твёрдые частицы | Капли жидкости | Пузырьки газа | |
| В тв\рдом теле | Сплав, композит, покрытие, плёнка | Твёрдая эмульсия | Твёрдая пена, фильтр, сорбент, мембрана |
| В жидкости | Суспензия | Эмульсия, крем | Пена |
| В газе | Аэрозоль, дым, пыль | Туман, капли | — |
Разделение смесей
Основные способы выделения веществ из неоднородной (гетерогенной) смеси:
- отстаивание;
- декантация;
- инерционная (гравитационная) сепарация;
- центрифугирование;
- фильтрование;
- флотация;
- магнитная сепарация.
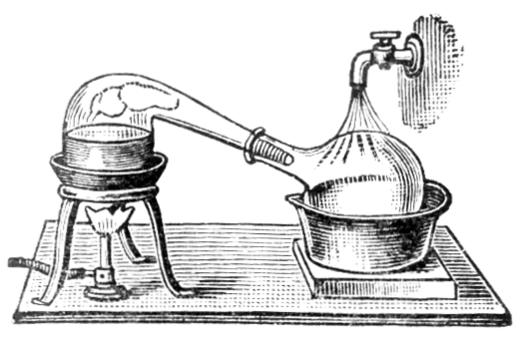
Основные способы выделения веществ из однородной (гомогенной) смеси:
Примечания
- ↑ 1 2 Ходаков Ю. В. Общая и неорганическая химия. Издательство Академии педагогических наук СССР (1954). Дата обращения: 9 мая 2025.
- ↑ The International Union of Pure and Applied Chemistry (IUPAC). mixture (англ.) // The IUPAC Compendium of Chemical Terminology. — Research Triangle Park, NC: International Union of Pure and Applied Chemistry (IUPAC), 2014-02-24. — doi:10.1351/goldbook.M03949.
- ↑ Глинка Н. Л. Общая химия. — Л.: Химия, 1984. — 704 с.
- ↑ 1 2 Жуков С. Т. Химия 8-9 класс. www.chem.msu.su. Дата обращения: 9 мая 2025.
- ↑ The International Union of Pure and Applied Chemistry (IUPAC). constituent (англ.) // The IUPAC Compendium of Chemical Terminology. — Research Triangle Park, NC: International Union of Pure and Applied Chemistry (IUPAC), 2019. — doi:10.1351/goldbook.C01281.
- ↑ The International Union of Pure and Applied Chemistry (IUPAC). constituent (англ.) // The IUPAC Compendium of Chemical Terminology. — Research Triangle Park, NC: International Union of Pure and Applied Chemistry (IUPAC), 2019. — doi:10.1351/goldbook.C01281.
- ↑ Герасимов И. Я. Курс физической химии. — М.: Химия, 1970.
- ↑ Ерёмин В. В. Основы физической химии. Теория и задачи. Internet Archive. Дата обращения: 9 мая 2025.
- ↑ Вольхин В. В. Общая химия. Основы химии.. — Пермь: Пермский государственный технический университет, 2001. — 512 с.
- ↑ WebCite query result (англ.). www.webcitation.org. Дата обращения: 9 мая 2025.
Литература
- Большая Советская Энциклопедия / Гл. ред. А. М. Прохоров. — 3-е изд. — М.: Советская Энциклопедия, 1975. — Т. 19: Проба — Ременсы. — 640 с.
- Вольхин В. В. Общая химия. Основы химии. — Пермь: Перм. гос. тех. ун-т, 2002. — 512 с. — ISBN 5-88151-309-6.
- Герасимов Я. И., Древинг В. П., Еремин Е. Н. и др. Курс физической химии / Под общ. ред. Я. И. Герасимова. — 2-е изд. — М.: Химия, 1970. — Т. I. — 592 с.
- Глинка Н. Л. Общая химия. Учебник для бакалавров / Под ред. В. А. Попкова и А. В. Бабкова. — 19-е изд., перераб. и доп. — М.: Юрайт, 2014. — 910 с. — (Бакалавр. Базовый курс). — ISBN 978-5-9916-3158-7.
- Еремин В. В., Каргов С. И., Успенская И. А. и др. Основы физической химии. Теория и задачи. — М.: Экзамен, 2005. — 481 с. — (Классический университетский учебник). — ISBN 5-472-00834-4.
- Коган В. Е., Литвинова Т. Е., Чиркст Д. Э., Шахпаронова Т. С. Физическая химия / Науч. ред. проф. Д. Э. Чиркст. — СПб.: Национальный минерально-сырьевой ун-т «Горный», 2013. — 450 с.
- Мечковский Л. А., Блохин А. В. Химическая термодинамика. Курс лекций. В двух частях. Часть 1. Феноменологическая термодинамика. Основные понятия, фазовые равновесия. — Минск: БГУ, 2010. — 141 с.
- Новиков И. И., Зайцев В. М. Термодинамика в вопросах и ответах. — М.: Госатомиздат, 1961. — 144 с.
- Путилов К. А. Термодинамика / Отв. ред. М. Х. Карапетьянц. — М.: Наука, 1971. — 376 с.
- Рудзитис Г. Е., Фельдман Ф. Г. Химия. Учебное пособие для 7—11 классов вечерней (сменной) средней общеобразовательной школы. В 2-х частях. Часть I. — М.: Просвещение, 1985. — 192 с.
- Рудзитис Г. Е., Фельдман Ф. Г. Химия. Неорганическая химия. 8 класс. — 15-е изд. — М.: Просвещение, 2011. — 176 с. — ISBN 978-5-09-025532-5.
- Сивухин Д. В. Общий курс физики. Т. II. Термодинамика и молекулярная физика. — 5-е изд., испр. — М.: ФИЗМАТЛИТ, 2005. — 544 с. — ISBN 5-9221-0601-5.
- Химическая энциклопедия / Гл. ред. Н. С. Зефиров. — М.: Большая Российская энциклопедия, 1995. — Т. 4: Пол — Три. — 640 с. — ISBN 5-85270-092-4.
- Ходаков Ю. В. Общая и неорганическая химия. Книга для учителя. — М.: Изд. Академии пед. наук РСФСР, 1954. — 524 с.
- Ходаков Ю. В., Эпштейн Д. А., Глориозов П. А. и др. Преподавание неорганической химии в средней школе. Методическое пособие для учителей. — М.: Просвещение, 1975. — 416 с. — (Методическая библиотека школы).