Скатол
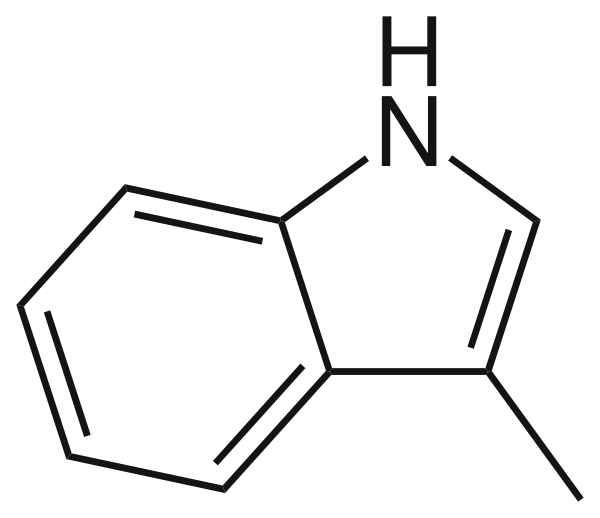
Скато́л (от др.-греч. σκῶρ, род. п. σκατός «экскременты»[1], 3-метилиндол, 4-метил-2,3-бензпиррол) — органическое гетероциклическое соединение, производное индола (в-метилиндол). Бесцветные кристаллы с очень неприятным запахом, напоминающим запах кала.
Общие сведения
| Скатол | |
|---|---|
| Общие | |
| Систематическое наименование |
3-метилиндол, 4-метил-2,3-бензпиррол |
| Традиционные названия | скатол |
| Хим. формула | C9H9N |
| Физические свойства | |
| Состояние |
бесцветные кристаллы, постепенно коричневеют |
| Молярная масса | 131,172 г/моль |
| Термические свойства | |
| Температура | |
| • плавления | 93—95 °C |
| • кипения | 265 °C |
| Химические свойства | |
| Растворимость | |
| • в воде | нерастворим |
| Классификация | |
| Рег. номер CAS | 83-34-1 |
| 3D model (JSmol) | Интерактивная схема |
| PubChem | 6736 |
| UNII | 9W945B5H7R |
| CompTox Dashboard EPA | DTXSID8021775 |
| Рег. номер EINECS | 201-471-7 |
| SMILES | |
| InChI | |
| ChEBI | 9171 |
| ChemSpider | 6480 |
| ECHA InfoCard | 100.001.338 |
Нахождение в природе
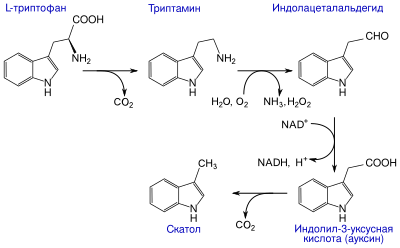
Скатол образуется в кишечнике человека и животных в результате разложения триптофана — одной из α-аминокислот, входящих в состав белков. Запах фекалий обусловлен, главным образом, содержанием в них скатола. Схема биосинтеза скатола в организме:
Поскольку триптофаном богаты белки животного происхождения (мясо), концентрация скатола в испражнениях возрастает при большом количестве мяса в рационе.
Установлено присутствие незначительных количеств скатола во многих цветочных эссенциях.
Скатол содержится в каменноугольной смоле, образуется при гниении белков.
Свойства
В больших концентрациях имеет фекальный запах (при низких концентрациях приобретает приятный сливочно-молочный запах или запах, напоминающий запах жасмина).
Порог восприятия запаха скатола человеком в воздухе крайне низкий. В литературе указываются значения 1,5 мкг/м3[2]; от 0,0005 до 6,4 мкг/м3[3]. Порог запаха в воде составляет 10 мкг/л[4]. В подсолнечном масле 15,6 ppb (частей на миллиард}[5].
Растворим в этаноле, хлороформе, диэтиловом эфире, бензоле. Температура плавления 93—95 °C.
Скатол обладает как слабоосновными, так и слабокислотными свойствами. Протоны метильной группы скатола обладают повышенной реакционной способностью, что определяет взаимодействие скатола с альдегидами. Скатол восстанавливается цинком в соляной кислоте до 2,3-дигидроскатола.
Качественной реакцией на скатол является фиолетовое окрашивание с реактивом Эрлиха.
Некоторые производные скатола: хлоргидрат, температура плавления 167—168 °C, и пикрат, температура плавления 170—171 °C.
Методы синтеза
Для получения скатола используют реакции Рейссерта или Фишера. Может быть получен по Фишеру из пропионового альдегида и фенилгидразина.
Применение
Используется как ароматизатор в парфюмерии, пищевой промышленности и как ароматизатор при производстве табачных изделий.
Безопасность
Сообщалось, что скатол вызывает отёк легких у мышей, крыс, овец и коз. Избирательно воздействует на клетки Клара в бронхах — основные резервуары фермента цитохрома P450, который превращает скатол в 3-метиленендоленин, повреждающий клетки вследствие образования комплексов с белками[6].
Примечания
Литература
- Химическая энциклопедия / Редкол.: Кнунянц И. Л. и др. — М.: Советская энциклопедия, 1995. — Т. 4 (Пол-Три). — 639 с. — ISBN 5-82270-092-4.
Ссылки
- The last word, NewScientist Health, 20 March 2004, issue 2439. Mark Gilkey, Palo Alto, California, US
- skatole (CHEBI:9171)
- 3-METHYLINDOLE