Пиросеквенирование
Пиросеквени́рование — это метод секвенирования ДНК (определение последовательности нуклеотидов в молекуле ДНК), основанный на принципе «секвенирование путём синтеза». При включении нуклеотида происходит детекция высвобождающихся пирофосфатов[1]. Технология была разработана Полом Ниреном (швед. Pål Nyrén) и его студентом Мустафой Ронаги англ. Mostafa Ronaghi) в Королевском технологическом институте (Стокгольм) в 1996 году[2][3][4].
Процедура
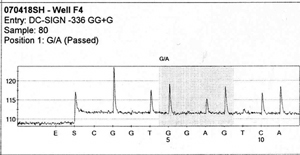
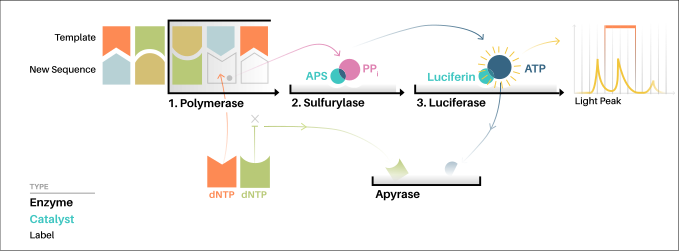
Идея пиросеквенирования заключается в регистрации пирофосфата, который образуется при присоединении очередного нуклеотида ДНК-полимеразой. Детекция пирофосфата осуществляется за счёт каскада химических реакций, который заканчивается выделением кванта света[5].
Прежде всего создаётся иммобилизованная на твёрдой фазе клональная библиотека одноцепочечных фрагментов ДНК (например, при помощи мостиковой полимеразной цепной реакции, ПЦР). Ко всем фрагментам ДНК присоединяется адаптер, с которым будет комплементарно связываться праймер — затравка для синтеза комплементарной цепи ДНК-полимеразой. Далее производится серия последовательных циклов, в процессе которых к закреплённой на твёрдой фазе ДНК по очереди добавляют дезоксинуклеотидтрифосфаты всех четырёх типов: A, T, G, C. Если на секвенируемой цепи ДНК есть комплементарный к добавленному нуклеотид, то при образовании фосфодиэфирной связи побочным продуктом станет пирофосфат. Он активирует каскад химических реакций: пирофосфат вместе с аденозинсульфофосфатом (АСФ) при помощи фермента АТФ-сульфурилазы образуют АТФ, который является источником энергии для проведения реакции окисления люциферина в оксилюциферин с выделением кванта света. Интенсивность выделяемого света пропорциональна числу включённых в цепь нуклеотидов (чем больше подряд одинаковых нуклеотидов, тем сильнее световой сигнал). Детекция света осуществляется ПЗС-матрицей и анализируется с помощью программного обеспечения, которое строит по пирограмме последовательность нуклеотидов. Нуклеотиды, не вовлечённые в синтез новой цепи, а также АТФ разрушаются ферментом апиразой. После этого начинается следующий цикл, то есть добавляется нуклеотид другого типа[6].
Позднее Маргулис и соавторы предложили сочетание пиросеквенирования с эмульсионной ПЦР[7].
Коммерциализация
Компания Pyrosequencing AB, которая располагается в Уппсале, Швеция, коммерциализовала технологию и реагенты для секвенирования коротких участков ДНК. В 2003 году Pyrosequencing AB переименована в «Biotage». В 2008 году Qiagen приобрел Biotage[8]. На принципе пиросеквенирования основана коммерческая технология 454 Life Sciences (компания Roche Applied Science)[7].
Достоинства и недостатки
По сравнению с секвенированием по Сэнгеру, пиросеквенирование выгодно отличается стоимостью, а также тем, что за один раз можно получить сотни тысяч прочтений. Однако пиросеквенирование имеет и ряд недостатков. Так, с помощью этого метода невозможно безошибочно секвенировать протяжённые участки, состоящие из одного и того же нуклеотида. Кроме того, оно позволяет получать лишь прочтения небольшой длины. Четвёртое поколение технологий пиросеквенирования, например, GS FLX Titanium, позволяет получать прочтения длиной более 400 пар оснований[9].
Литература
- Д. В. Ребриков, Д. О. Коростин, Е. С. Шубина, В. В. Ильинский. NGS: высокопроизводительное секвенирование / под общей редакцией Д. В. Ребрикова. — М.: БИНОМ. Лаборатория знаний, 2015. — 232 с. — ISBN 978-5-9963-0373-1.
Примечания
Ссылки
- Натальин, Павел. 454-секвенирование (высокопроизводительное пиросеквенирование ДНК). // Сайт Biomolecula.ru (6 февраля 2008). Дата обращения: 21 марта 2018. Архивировано 7 апреля 2018 года.
- Недолужко, Артём; Пташник, Ольга. 12 методов в картинках: секвенирование нуклеиновых кислот. // Сайт Biomolecula.ru (11 августа 2017). Дата обращения: 21 марта 2018.