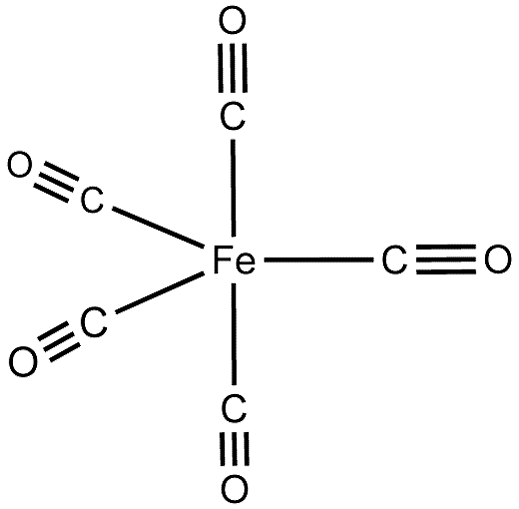
Пентакарбонилжелезо
Пентакарбонилжелезо — неорганическое соединение, карбонильный комплекс железа состава [Fe(CO)5]. Светло-жёлтая жидкость, не смешивается с водой.
Общие сведения
| Пентакарбонилжелезо | |
|---|---|
| Общие | |
| Систематическое наименование |
Пентакарбонилжелезо |
| Традиционные названия | Пентакарбонил железа |
| Хим. формула | [Fe(CO)5] |
| Физические свойства | |
| Состояние | светло-жёлтая жидкость |
| Молярная масса | 195,90 г/моль |
| Плотность | 1,457; 1,4664 г/см³ |
| Термические свойства | |
| Температура | |
| • плавления | -21; -20 °C |
| • кипения | 102,5; 103; 104,9 °C |
| • вспышки | 5 ± 1[1] |
| Давление пара | 40 ± 1[1], 1 ± 1[2], 10 ± 1[2] и 100 ± 1[2] |
| Оптические свойства | |
| Показатель преломления | 1,453 ± 0,001[3] и 1,523 ± 0,001[4] |
| Классификация | |
| Рег. номер CAS | 13463-40-6 |
| 3D model (JSmol) | Интерактивная схема |
| PubChem | 26040 |
| UNII | 6WQ62TAQ6Z |
| CompTox Dashboard EPA | DTXSID3027746 |
| Рег. номер EINECS | 236-670-8 |
| SMILES | |
| InChI | |
| RTECS | NO4900000 |
| ChEBI | CHEBI:30251 |
| Номер ООН | 1994 |
| ChemSpider | 24254 |
| ECHA InfoCard | 100.033.323 |
| Безопасность | |
| Предельная концентрация | 0,8 мг/кг |
| ЛД50 | 25 мг/кг |
| Токсичность | Высокотоксичен, СДЯВ |
| Пиктограммы ECB |
|
| NFPA 704 | |
Получение
- Действие монооксида углерода под давлением на порошок железа:
- Действие монооксида углерода под давлением на иодид железа(II) и медь:
- Разложение при нагревании нонакарбонилдижелеза:
Физические свойства
Пентакарбонилжелезо образует светло-жёлтую диамагнитную жидкость, не смешивается с холодной водой, растворяется в этаноле, диэтиловом эфире, ацетоне, бензоле, уксусной кислоте.
Химические свойства
- Разлагается при нагревании:
- Реагирует с горячей водой:
- Реагирует с кислотами (в диэтиловом эфире):
- Окисляется кислородом:
- Реагирует с иодистоводородной кислотой:
- При облучении ультрафиолетовым светом раствора в уксусной кислоте образуются высшие карбонилы:
- Под действием катализатора алкоголята натрия на раствор в этаноле образуются высшие карбонилы:
- Реагирует с основаниями в метаноле:
- Реагирует с монооксидом азота под давлением:
Применение
- Для получения порошка железа.
- В качестве катализатора.
- В качестве восстановителя в органическом синтезе.[5]
Физиологические свойства
- Пентакарбонил железа [Fe(CO)5] высокотоксичен, как и многие другие карбонилы металлов. Сильнейший неорганический яд.
- ПДК = 0,8 мг/м³.
- ЛД50 = 25 мг/кг.
- Очень опасен для окружающей среды.
Примечания
Литература
- Химическая энциклопедия / Редкол.: Кнунянц И.Л. и др.. — М.: Советская энциклопедия, 1990. — Т. 2. — 671 с. — ISBN 5-82270-035-5.
- Справочник химика / Редкол.: Никольский Б.П. и др.. — 3-е изд., испр. — Л.: Химия, 1971. — Т. 2. — 1168 с.
- Лидин Р.А. и др. Химические свойства неорганических веществ: Учеб. пособие для вузов. — 3-е изд., испр. — М.: Химия, 2000. — 480 с. — ISBN 5-7245-1163-0.
- Рипан Р., Четяну И. Неорганическая химия. Химия металлов. — М.: Мир, 1972. — Т. 2. — 871 с.
- Неорганическая химия / под ред. Ю.Д. Третьякова. — М.: Академия, 2007. — Т. 3. — 400 с.













![{\displaystyle {\mathsf {Fe(CO)_{5}+3NaOH{\xrightarrow {}}\ Na[HFe(CO)_{4}]+NaHCO_{3}}}}](https://ru.ruwiki.ru/api/rest_v1/media/math/render/svg/c3bf5b30a131e45c2aafab2042a7f8775cdd3d28)
![{\displaystyle {\mathsf {Fe(CO)_{5}+Ba(OH)_{2}{\xrightarrow {-15^{o}C}}\ [Fe(CO)_{4}H_{2}]+BaCO_{3}\downarrow }}}](https://ru.ruwiki.ru/api/rest_v1/media/math/render/svg/801ad9419ffac154c4429f3be78179bacfd16151)
![{\displaystyle {\mathsf {Fe(CO)_{5}+2Na{\xrightarrow {-40^{o}C}}\ Na_{2}[Fe(CO)_{4}]\downarrow +CO\uparrow }}}](https://ru.ruwiki.ru/api/rest_v1/media/math/render/svg/2d1dd77205525afb19cdc839c61218b085c4e52d)
![{\displaystyle {\mathsf {Fe(CO)_{5}+4NO{\xrightarrow {45^{o}C}}\ [Fe(NO)_{4}]+5CO\uparrow }}}](https://ru.ruwiki.ru/api/rest_v1/media/math/render/svg/14d9cce5b08541a015b1d0c72165b6faa39a7889)