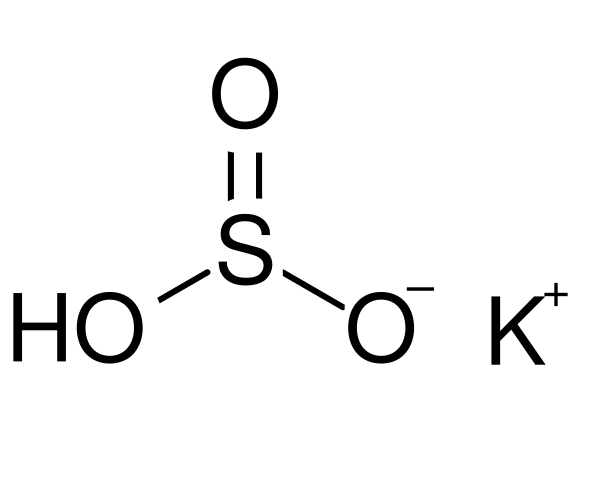
Гидросульфит калия
Гидросульфи́т ка́лия — неорганическое соединение, кислая соль щелочного металла калия и сернистой кислоты с формулой , бесцветные кристаллы, растворимые в воде. Зарегистрирован в качестве пищевой добавки с номером Е228.
Общие сведения
| Гидросульфит калия | |
|---|---|
| Общие | |
| Систематическое наименование |
Гидросульфит калия |
| Традиционные названия | Сернистокислый калий кислый; бисульфит калия |
| Хим. формула | KHSO3 |
| Физические свойства | |
| Состояние | бесцветные кристаллы |
| Молярная масса | 120,17 г/моль |
| Термические свойства | |
| Температура | |
| • плавления | разр. 190 °C |
| Химические свойства | |
| Растворимость | |
| • в воде | 4920; 115100 г/100 мл |
| Классификация | |
| Рег. номер CAS | 7773-03-7 |
| 3D model (JSmol) | Интерактивная схема |
| PubChem | 23663620 |
| UNII | QJK5LO891P |
| CompTox Dashboard EPA | DTXSID6064795 |
| Рег. номер EINECS | 231-870-1 |
| SMILES | |
| InChI | |
| Кодекс Алиментариус | E228 |
| ChemSpider | 22889 |
| ECHA InfoCard | 100.028.973 |
Получение
- Насыщение диоксидом серы раствора гидроксида калия, карбоната калия или сульфита калия:
Физические свойства
Гидросульфит калия образует бесцветные кристаллы, растворимые в воде, плохо растворимы в этаноле.
Водные растворы имеют кислую реакцию.
Химические свойства
- При нагревании разлагается:
- Разлагается кислотами:
- Разлагается щелочами:
- Медленно окисляется кислородом воздуха:
Применение
- Пищевая добавка Е228 — консервант, запрещена к использованию в некоторых странах.
Безопасность
Управление по санитарному надзору за качеством пищевых продуктов и медикаментов (FDA) признаёт гидросульфит калия как «общепризнанную безопасную» (GRAS) пищевую добавку в США, за исключением его использования в продуктах, признанных источником витамина B1 (тиамина), поскольку гидросульфит калия (наряду с добавками Е220-Е228) разлагает этот микронутриент и его использование в перечне богатых витамином B1 продуктов, а также во фруктах и овощах запрещено[1].
Объединённый экспертный комитет ФАО/ВОЗ по пищевым добавкам (JECFA), проводя исследования безопасности гидросульфита калия в качестве пищевой добавки, не смог определить допустимое суточное потребление (ДСП) в 1985 году[2]. В 2016 году, Европейское агентство по безопасности продуктов питания (EFSA), проводя переоценку безопасности, установило ДСП в количестве 0,7 мг/кг массы тела (в пересчёте с диоксида серы)[3].
Примечания
Литература
- Справочник химика / Редкол.: Никольский Б.П. и др.. — 3-е изд., испр. — Л.: Химия, 1971. — Т. 2. — 1168 с.
- Лидин Р.А. и др. Химические свойства неорганических веществ: Учеб. пособие для вузов. — 3-е изд., испр. — М.: Химия, 2000. — 480 с. — ISBN 5-7245-1163-0.
- Рипан Р., Четяну И. Неорганическая химия. Химия металлов. — М.: Мир, 1971. — Т. 1. — 561 с.