Виниловый спирт
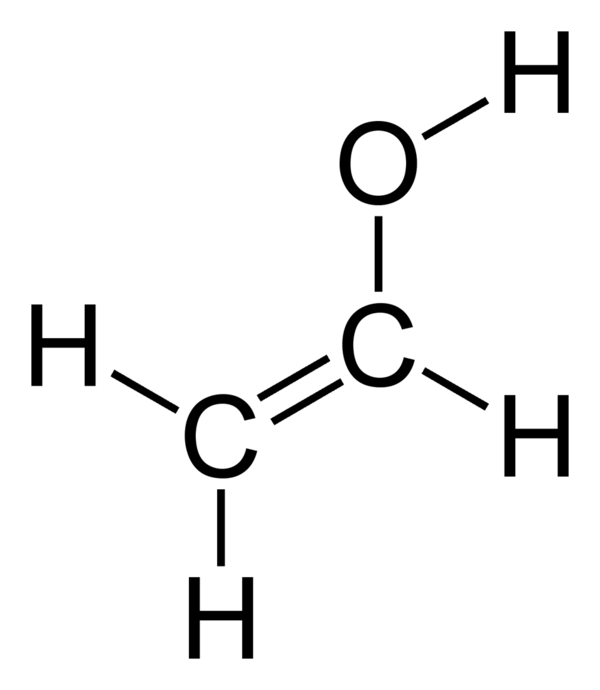
Виниловый спирт (этенол, не путать с этанолом) — ненасыщенный одноатомный спирт с формулой CH2=CH-OH, простейший енол, легко превращается в ацетальдегид. Получены его простые и сложные эфиры.
Общие сведения
| Виниловый спирт | |
|---|---|
| Общие | |
| Систематическое наименование |
Этенол |
| Традиционные названия | Виниловый спирт |
| Хим. формула | С2H4O |
| Физические свойства | |
| Молярная масса | 44,05 г/моль |
| Классификация | |
| Рег. номер CAS | [557-75-5] |
| 3D model (JSmol) | Интерактивная схема |
| PubChem | 11199 |
| CompTox Dashboard EPA | DTXSID8051467 |
| Рег. номер EINECS | 209-183-3 |
| SMILES | |
| InChI | |
| ChemSpider | 10726 |
| ECHA InfoCard | 100.008.350 |
Синтез
Виниловый спирт можно получить путём дегидратации этиленгликоля при температуре 900 °С и низком давлении[1].
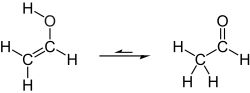
Таутомеризация винилового спирта в ацетальдегид
В нормальных условиях виниловый спирт таутомеризуется в ацетальдегид:
При комнатной температуре ацетальдегид более стабилен, чем виниловый спирт, энтальпия превращения составляет 42,7 кДж/моль.[2]
В отсутствие катализатора кето-енольная таутомерия за счёт миграции 1,3-водорода запрещена правилами Вудворда-Хоффмана, имеет высокий активационный барьер и затруднительна при комнатной температуре или около неё. Однако даже следовые количества кислот, оснований или воды могут катализировать реакцию. Даже при строгих мерах предосторожности, направленных на ликвидацию случайной влаги или источников протонов, виниловый спирт можно хранить только от нескольких минут до нескольких часов, прежде чем он изомеризуется в ацетальдегид. (Другим примером вещества, стабильного в строгой чистоте, но быстро разлагающегося из-за катализа следами влаги, является угольная кислота.)
Таутомеризация также может быть катализирована с помощью фотохимического процесса. Эти данные свидетельствуют о том, что кето-енольная таутомеризация легко протекает в атмосфере и стратосфере, и о том, что виниловый спирт играет роль в появлении органических кислот в атмосфере[4][5].
Виниловый спирт можно стабилизировать, контролируя концентрацию воды в системе и используя кинетический изотопный эффект, замедляющий реакции с участием дейтерия. Этого эффекта можно добиться путём гидролиза предшественника кетена в присутствии небольшого стехиометрического избытка тяжёлой воды (D2O). Исследования показывают, что процесс таутомеризации значительно ингибируется при температуре окружающей среды, а период полураспада енольной формы можно легко увеличить до t 1/2 = 42 мин[6].
Связь с поливиниловым спиртом
Из-за нестабильности винилового спирта термопластичный поливиниловый спирт (ПВС или PVOH) получают косвенно путём полимеризации винилацетата с последующим гидролизом сложноэфирных связей.
Лиганд
Получено несколько комплексов металлов, содержащих виниловый спирт в качестве лиганда, таких как Pt(acac)(η 2 -C 2 H 3 OH)Cl.[7]
См. также
Примечания
Литература
- Енолы // Большая Советская энциклопедия (в 30 т.) / А. М. Прохоров (гл. ред.). — 3-е изд. — М.: Сов. энциклопедия, 1972. — Т. IX. — С. 87. — 624 с.