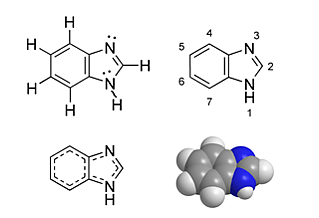
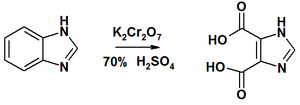Бензимидазол
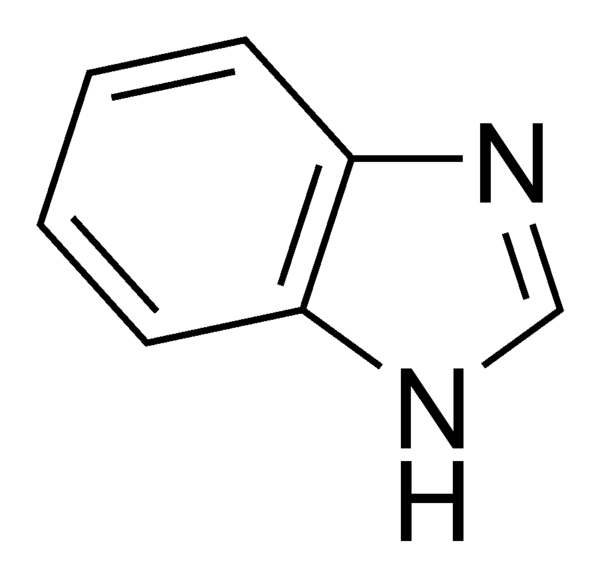
Бензимидазол — азотсодержащие ароматическое гетероциклическое соединение в структуру которого входят сопряжённые кольца бензола и имидазола.
Общие сведения
| Бензимидазол | |
|---|---|
| Общие | |
| Хим. формула | C7H6N2 |
| Физические свойства | |
| Молярная масса | 118,14 г/моль |
| Термические свойства | |
| Температура | |
| • плавления | 170–172 °C |
| • кипения | >360 °C |
| Химические свойства | |
| Константа диссоциации кислоты | 5,53 и 13,2 |
| Структура | |
| Дипольный момент | 4,02 Д |
| Классификация | |
| Рег. номер CAS | 51-17-2 |
| 3D model (JSmol) | Интерактивная схема |
| PubChem | 5798 |
| UNII | E24GX49LD8 |
| CompTox Dashboard EPA | DTXSID8024573 |
| Рег. номер EINECS | 200-081-4 |
| SMILES | |
| InChI | |
| RTECS | DD5425000 |
| ChEBI | 41275 |
| ChemSpider | 5593 |
| ECHA InfoCard | 100.000.075 |
Физические свойства
Получение
Лабораторный метод синтеза бензимидазола - реакция о-фенилендиамина с муравьиной кислотой[1][2], либо с триметилортоформиатом. 2-алкилбензимидазолы получаются взаимодействием жирных кислот с о-фенилендиамином в присутствии HCl[3]. 2-арилбензимидазолы получаются конденсацией о-фенилендиамина с ароматическими альдегидами с последующим окислением ацетатом меди (I) (реакция Вайденхагена).
Химические свойства
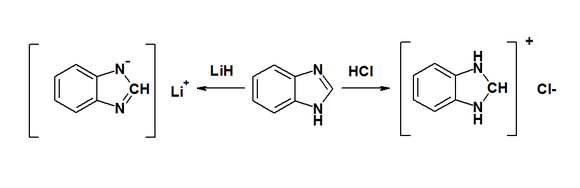
Проявляет амфотерные свойства,
образует с ионами некоторых переходных металлов (Ag, Cu) соли в аммиачном растворе.
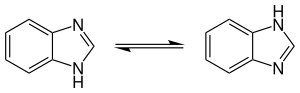
Вследствие таутомерии имидазольного цикла в бензимидазоле положения 4-7 и 5-6 бензольного цикла бензимидазола эквивалентны.
Бензимидазол алкилируется алкилгалогенидами и алкилсульфатами с образованием сначала 1-алкилбензимидазолов[4] и, затем, 1,3-диалкилбензимидазолиевых солей. Также бензимидазол легко аминометилируется под действием формальдегида и вторичного амина[5].
Под влиянием имидазольного фрагмента бензольное кольцо бензимидазола деактивировано по отношению к реакциям электрофильного замещения: так, бензимидазол нитруется смесью азотной и серной кислот с образованием 5-нитробензимидазола[6] и сульфируется с образованием смеси 5- и 6-бензимидазолилсульфокислот.
При сплавлении бензимидазола с серой образуется бензимидазол-2-тион. Окисление хроматом калия в 70% серной кислоте ведёт к деградации бензольного фрагмента с образованием имидазол-4,5-дикарбоновой кислоты[7].
Применение
Имидазол находил ограниченное применение в качестве подавителя вуалеобразования при проявлении галогенсеребряных фотоматериалов, в настоящее время практического значения не имеет. Вместе с тем, ряд производных бензимидазола являются биологически активными соединениями - N-рибозил-гликозид бензимидазола является аксиальным лигандом, координирующим кобальт в витамине B12.[8], ряд производных бензимидазола применяются в качестве фармацевтических препаратов (дибазол, омепразол, мебендазол и др.).
Токсичность
ЛД50 (крысы, перорально) - 2910 мг на кг.
См. также
Примечания
Литература
- Симонов А. В. Бензимидазол // Химическая энциклопедия : в 5 т. / Гл. ред. И. Л. Кнунянц. — М.: Советская энциклопедия, 1988. — Т. 1: А — Дарзана. — С. 261. — 623 с. — 100 000 экз. — ISBN 5-85270-008-8.