Candida albicans
Candida albicans — диплоидный диморфный грибок, наиболее известный и клинически значимый вид дрожжей рода Candida[4]. Является комменсалом и частью нормальной микрофлоры слизистых оболочек полости рта, пищеварительного тракта и урогенитальной системы у большинства здоровых людей[5]. При определённых условиях, в первую очередь при ослаблении иммунитета, C. albicans начинает активно размножаться, вызывая заболевание кандидоз[6]. C. albicans является возбудителем до 90 % случаев кандидоза[7].
Инфекции могут быть как поверхностными (поражение кожи и слизистых оболочек, например, молочница полости рта или вульвовагинит), так и системными (фунгемиями), которые представляют серьёзную угрозу для пациентов с иммунодефицитом (например, при СПИДе, химиотерапии рака или после трансплантации органов)[8][9]. Кроме того, этот грибок является одним из основных возбудителей внутрибольничных инфекций.
Общие сведения
Candida albicans | |||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| Научная классификация | |||||||||||||||
|
|||||||||||||||
| Латинское название | |||||||||||||||
| Candida albicans (C.P. Robin) Berkhout, 1923 |
Классификация
- Домен: Эукариоты (Eukaryota)
- Царство: Грибы (Fungi)
- Отдел: Аскомицеты (Ascomycota)
- Класс: Сахаромицеты (Saccharomycetes)[10]
- Порядок: Serinales
- Семейство: Debaryomycetaceae
- Род: Candida[10]
- Вид: Candida albicans
Современная таксономия C. albicans, основанная на молекулярно-генетических исследованиях, отличается от более ранних классификаций. Ранее вид относили к порядку Saccharomycetales и семейству Saccharomycetaceae[10]. Однако, согласно актуальным таксономическим базам данных, таким как NCBI, C. albicans был переклассифицирован в порядок Serinales[11] и семейство Debaryomycetaceae[12].
Морфология и биологические свойства
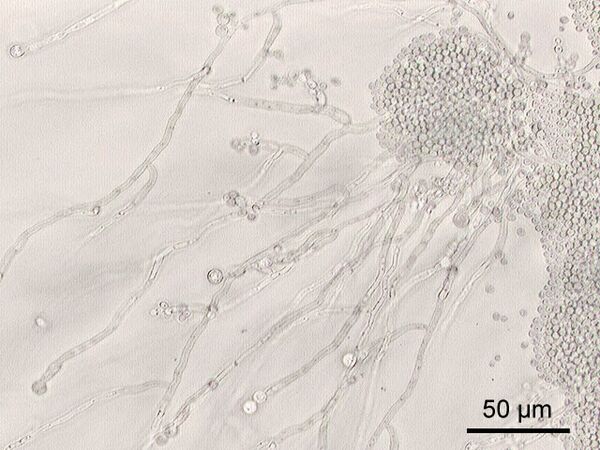
Одной из ключевых морфологических особенностей C. albicans является диморфизм — способность существовать в различных формах в зависимости от условий окружающей среды[13]. Основные формы:
- Дрожжевая форма (бластоспоры): одноклеточные овальные или сферические почкующиеся клетки размером 3—6 мкм[14]. Эта форма характерна для сапрофитного существования грибка.
- Псевдомицелий: образуется в результате незавершённого почкования, когда дочерние клетки не отделяются от материнской и удлиняются, формируя цепочки, напоминающие мицелий. На перетяжках между клетками располагаются скопления бластоспор[15].
- Истинный мицелий (гифы): в условиях, способствующих инвазии в ткани, C. albicans формирует длинные, септированные (разделённые перегородками) нити[16]. Характерным признаком вида является образование «ростковых трубок» (зародышевых гиф) при инкубации в сыворотке крови при 37 °C[14].
- Хламидоспоры: в неблагоприятных условиях на специальных средах грибок может образовывать крупные, толстостенные, двухконтурные покоящиеся споры[15].
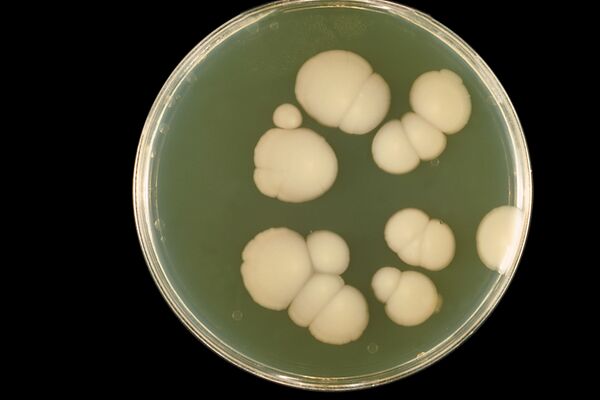
На плотных питательных средах, таких как агар Сабуро, C. albicans через 24—48 часов инкубации при температуре 25—37 °C образует выпуклые, блестящие, сметанообразные колонии белого или кремового цвета с характерным кисловатым запахом[14].
C. albicans является аэробом, для его роста и размножения необходим кислород. Оптимальными условиями для роста считаются температура 30—37 °C и слабокислая среда (pH 5,8—6,5). Грибок способен ферментировать и ассимилировать различные углеводы, в частности глюкозу и мальтозу, что используется в лабораторной диагностике для идентификации вида[15]. C. albicans обладает высокой способностью к адгезии (прикреплению) к эпителиальным клеткам[17] и может формировать биоплёнки — высокоструктурированные сообщества клеток, заключённые во внеклеточный матрикс. Биоплёнки повышают устойчивость грибка к противогрибковым препаратам и факторам иммунной системы[18].
Патогенность и клиническое значение
Патогенность C. albicans обусловлена набором факторов вирулентности, которые позволяют грибку прикрепляться к тканям хозяина, проникать в них, получать питательные вещества и уклоняться от иммунной системы[19]. Ключевые факторы включают:
- Адгезия. Является первым и критически важным этапом инфекционного процесса. C. albicans использует для прикрепления к эпителиальным и эндотелиальным клеткам, а также к медицинским имплантатам, специальные белки-адгезины, в частности, агглютинин-подобные белки (семейство Als) и белок Hwp1[20][19].
- Диморфизм. Способность переключаться между различными морфологическими формами играет центральную роль в патогенезе[20]. Одноклеточная дрожжевая форма способствует распространению (диссеминации) грибка в организме через кровоток, в то время как нитевидная (гифальная) форма необходима для активного проникновения (инвазии) в ткани хозяина и разрушения эпителиальных барьеров[19].
- Секреция гидролитических ферментов. Для проникновения в ткани и получения питательных веществ C. albicans выделяет ферменты, разрушающие клеточные структуры хозяина. К ним относятся секретируемые аспартатные протеиназы (Sap), которые разрушают белки, а также фосфолипазы и липазы, которые расщепляют компоненты клеточных мембран[20][19].
- Формирование биоплёнок. C. albicans способен формировать высокоструктурированные сообщества клеток, заключённые во внеклеточный матрикс. Биоплёнки могут образовываться как на слизистых оболочках, так и на поверхностях медицинских устройств (например, катетеров). Клетки в составе биоплёнки значительно более устойчивы к противогрибковым препаратам и действию иммунной системы хозяина[20], а сами биоплёнки служат резервуаром для хронических и рецидивирующих инфекций.
- Фенотипическое переключение. Грибок способен спонтанно и обратимо изменять внешний вид своих колоний. Эти изменения связаны с вариациями в антигенной структуре поверхности клетки, что позволяет C. albicans уклоняться от иммунного ответа хозяина и адаптироваться к различным условиям внутри организма[21][22].
При ослаблении защитных сил организма C. albicans вызывает заболевание кандидоз. Проявления кандидоза зависят от места поражения и делятся на две основные группы: поверхностные и инвазивные (системные).
Поверхностный кандидоз (поражение кожи и слизистых оболочек):
- Кандидоз полости рта (молочница): Проявляется в виде белых, творожистых пятен на слизистой оболочке рта, которые при попытке соскоблить могут кровоточить. Часто встречается у младенцев и людей с ослабленным иммунитетом[23].
- Кандидоз пищевода: Вызывает боль при глотании (дисфагия) и является одним из признаков СПИДа[24].
- Урогенитальный кандидоз: У женщин (вульвовагинит) сопровождается зудом, жжением и белыми творожистыми выделениями. У мужчин (баланит, баланопостит) характеризуется зудом, покраснением и белым налётом на головке полового члена[25].
- Кандидоз кожи: Обычно развивается в кожных складках (подмышечные впадины, паховая область), где тепло и влажно, и проявляется в виде сыпи и зуда.
Инвазивный (системный) кандидоз Это тяжёлая форма заболевания, при которой грибок проникает в кровоток (кандидемия) и распространяется по всему организму, поражая внутренние органы. Инвазивный кандидоз развивается преимущественно у людей с серьёзным ослаблением иммунитета.
- Кандидемия (кандидозный сепсис): Наличие грибка в крови, сопровождающееся лихорадкой, которая не спадает на фоне приёма антибиотиков[26].
- Поражение внутренних органов: C. albicans может поражать почки, печень, головной мозг, сердце, лёгкие и глаза, что приводит к нарушению их функций и может быть смертельно опасно.
Развитию кандидоза способствуют следующие факторы риска:
- Снижение иммунитета: Врождённые или приобретённые иммунодефицитные состояния, такие как ВИЧ/СПИД, онкологические заболевания, а также приём препаратов, подавляющих иммунную систему (иммуносупрессанты, кортикостероиды)[27].
- Длительный или бесконтрольный приём антибиотиков: Уничтожение нормальной микрофлоры, которая в норме сдерживает рост Candida[27].
- Эндокринные заболевания: В первую очередь сахарный диабет, так как повышенный уровень сахара в крови создаёт благоприятную среду для размножения грибка[28].
- Гормональные изменения: Беременность, приём гормональных контрацептивов или менопауза.
- Медицинские вмешательства: Наличие венозных катетеров, хирургические операции и парентеральное питание являются факторами риска для развития инвазивного кандидоза[29].
- Неправильное питание и вредные привычки: Недостаток витаминов и минералов, злоупотребление алкоголем[28].
Диагностика
Диагностика кандидоза и идентификация возбудителя включают комплекс методов, выбор которых зависит от локализации поражения и клинической картины[30].
- Микроскопическое исследование. Один из основных и быстрых способов диагностики[31]. Из поражённых участков (кожи, слизистых оболочек) берётся соскоб или мазок, который исследуется под микроскопом. Диагностическим признаком является обнаружение элементов гриба: почкующихся дрожжеподобных клеток и нитей псевдомицелия[32].
- Культуральный (микологический) метод. Считается «золотым стандартом» в диагностике кандидоза[33]. Биологический материал высевают на специальные питательные среды, например, на агар Сабуро[25]. Метод позволяет не только подтвердить наличие грибов рода Candida, но и определить их количество, а также идентифицировать вид возбудителя[33]. Кроме того, он даёт возможность определить чувствительность выделенного грибка к противогрибковым препаратам для подбора эффективной терапии[34].
- ПЦР. Современный и высокочувствительный молекулярно-генетический метод, который выявляет ДНК грибов Candida в исследуемом материале. ПЦР-диагностика позволяет не только обнаружить возбудителя, но и точно определить его вид (C. albicans, C. glabrata и др.). Метод отличается высокой скоростью получения результата и способностью выявлять инфекцию даже при небольшом количестве грибков[35].
- Серологические тесты (ИФА). Направлены на выявление в крови антител к антигенам грибов рода Candida[31]. Этот метод чаще используется при диагностике инвазивных (системных) форм кандидоза. Однако обнаружение антител не всегда свидетельствует об активной инфекции, так как они могут присутствовать и у здоровых носителей.
Помимо общих методов, для видовой идентификации именно C. albicans используются специфические тесты, такие как тест на образование «зародышевых трубок» (Germ tube test) в сыворотке крови и выявление образования хламидоспор на специальных средах.
Важно отметить, что обнаружение грибов рода Candida, особенно в небольшом количестве, не всегда является признаком заболевания, так как они входят в состав нормальной микрофлоры. Диагноз «кандидоз» ставится врачом на основании совокупности данных: клинических проявлений и результатов лабораторных исследований[33].
Лечение
Лечение кандидоза зависит от локализации и степени тяжести инфекции. Подход к терапии варьируется от местного применения препаратов при поверхностных поражениях до системного лечения при инвазивных формах заболевания[31].
При поражении кожи и слизистых оболочек, применяются местные или пероральные противогрибковые препараты[31].
- Кандидоз полости рта (молочница): Лечение включает применение местных противогрибковых средств в виде растворов, гелей или таблеток для рассасывания. В более тяжёлых случаях назначают системные препараты, такие как флуконазол[36].
- Кандидоз кожи: Поражения обычно локализуются в кожных складках. Для лечения используются противогрибковые кремы и мази[37].
- Вульвовагинальный кандидоз: Применяются местные средства в виде вагинальных свечей, таблеток или кремов (например, с клотримазолом, миконазолом)[36]. При рецидивирующем течении может быть назначен курсовой приём флуконазола внутрь[38].
- Кандидоз желудочно-кишечного тракта: При неинвазивных формах могут использоваться препараты, которые плохо всасываются из кишечника, но оказывают сильное местное действие, например, нистатин или натамицин[37].
Инвазивный кандидоз — это тяжёлое состояние, при котором грибок попадает в кровоток (кандидемия) и поражает внутренние органы. Такое состояние требует немедленного системного лечения, как правило, в условиях стационара.
- Препараты первого ряда: Для пациентов в критическом состоянии рекомендовано начинать лечение с эхинокандинов (каспофунгин, микафунгин, анидулафунгин), которые вводятся внутривенно[39].
- Альтернативная терапия: В качестве стартовой терапии также может использоваться амфотерицин B[37].
- Важный аспект лечения: При кандидемии у пациентов с установленными внутривенными катетерами рекомендуется их удаление.
Лечение кандидоза проводится с использованием нескольких классов антимикотиков:
- Азолы:
- Триазолы: флуконазол, итраконазол, вориконазол. Широко применяются для лечения как поверхностных, так и системных форм кандидоза.
- Имидазолы: кетоконазол, клотримазол, миконазол. В основном используются местно для лечения кожных и слизистых инфекций[37].
- Полиены:
- Амфотерицин B: Мощный препарат для лечения тяжёлых системных грибковых инфекций.
- Нистатин, Натамицин: Применяются в основном для лечения кандидоза кожи, слизистых оболочек и ЖКТ[37].
- Эхинокандины:
- Каспофунгин, микафунгин, анидулафунгин: Эффективны при лечении инвазивного кандидоза, вводятся внутривенно[40].
- Другие группы: В некоторых случаях, обычно в комбинации с другими средствами, может применяться флуцитозин.
Выбор конкретного препарата, его дозировки и длительности лечения должен осуществляться исключительно врачом на основании диагноза, тяжести заболевания и чувствительности грибка[36].
Научные исследования
В 2024 году научные исследования были сосредоточены на изучении механизмов патогенеза и способов уклонения C. albicans от иммунной системы. В сентябре было опубликовано исследование, раскрывшее, что грибок выделяет эффекторный белок Cmi1, который проникает в клетки иммунной системы и подавляет противогрибковый ответ, воздействуя на белок TBK1[41]. Ранее, в январе, анализ около 2000 геномов шести основных видов Candida выявил сотни генов, подвергшихся быстрой селекции, что указывает на активную адаптацию патогена к человеку и противогрибковым препаратам[42]. В августе исследователи из университетов Бирмингема и Кента получили крупный грант на изучение стратегий адаптации грибка с целью поиска новых терапевтических мишеней[43].
Значительное внимание было уделено инновационным подходам к лечению и профилактике. В марте в Journal of Experimental Medicine были опубликованы результаты исследования, в ходе которого была открыта новая разновидность дрожжей — Kazachstania weizmannii. Было показано, что этот вид способен вытеснять C. albicans из кишечника, успешно конкурируя с ним за ресурсы, что открывает перспективы для разработки пробиотической терапии[44]. В июне учёные из Калифорнийского университета в Дейвисе обнаружили, что противовоспалительный препарат месаламин (5-ASA) может подавлять рост грибка в кишечнике, поддерживая неблагоприятный для него низкий уровень кислорода[45]. Также в мае был опубликован обзор, систематизирующий данные об использовании эфирных масел как перспективного направления для разработки альтернативных противогрибковых средств на фоне растущей лекарственной устойчивости[46].
Продолжалась работа и над созданием новых противогрибковых препаратов. В обзоре от марта 2024 года отмечался прогресс в разработке таких средств, как резафунгин, ибрексафунгерп и фосманогепикс. В частности, резафунгин в январе получил в Европе статус орфанного препарата, что должно ускорить его внедрение в клиническую практику[47].
В 2025 году научные исследования были сосредоточены на преодолении растущей лекарственной устойчивости C. albicans. Ключевые открытия включали обнаружение нового класса противогрибковых препаратов, разработку инновационных терапевтических методик и выявление ранее неизвестных механизмов патогенности.
В августе 2025 года исследователи из Университета Макмастера объявили об открытии нового класса противогрибковых молекул — кониотинов. Эти соединения, выделенные из гриба Coniochaeta hoffmannii, эффективно разрушают клеточную стенку C. albicans. Открытие, опубликованное в журнале Nature Communications, считается значительным прорывом, так как может пополнить ограниченный арсенал существующих классов противогрибковых средств[48]. В том же месяце учёные из Бразилии представили метод борьбы с биоплёнками C. albicans с помощью фотодинамической терапии. Методика использует куркумин, активируемый синим светом лазера, для выработки активных форм кислорода, которые разрушают как клетки грибка, так и его защитный матрикс. Комбинация терапии с противогрибковым препаратом показала подавление роста патогена на 87,5 %[49].
В июле международная группа под руководством Института Лейбница выявила ранее неизвестный механизм патогенности. Было обнаружено, что C. albicans может использовать человеческий сывороточный альбумин для активации своей вирулентности. Штаммы, считавшиеся безвредными в лабораторных условиях, в присутствии альбумина становились цитотоксичными и способными повреждать ткани человека. Это открытие, также опубликованное в Nature Communications, объясняет, почему некоторые клинические штаммы вызывают инфекции, несмотря на кажущуюся безопасность в стандартных тестах[50][51]. Кроме того, в 2025 году были опубликованы обзоры, указывающие на рост числа инвазивных кандидозов как осложнений после перенесённой инфекции COVID-19, особенно у пациентов с ослабленным иммунитетом[52].