Теиксобактин
Теиксобактин (англ. Teixobactin) — антибиотик, который активен в отношении патогенных грамположительных бактерий, выработавших резистентность к существующим утверждённым антибиотикам. Об открытии было объявлено в январе 2015 года. Антибиотик был обнаружен при скрининге некультивируемых почвенных бактерий, выращенных in situ в устройстве для культивации бактерий ichip с помощью методов, разработанных учеными Северо-Восточного университета Бостона, штат Массачусетс, США.
Первые клинические исследования на людях начнутся не ранее 2017 года[1]. По заявлению биоинформатика Павла Певзнера теиксобактин, скорее всего, является антибиотиком нового класса, который проходит клинические испытания по состоянию на 2019 год. Выход нового антибиотика на рынок занимает порядка 10 лет с момента его открытия.
Общие сведения
| Теиксобактин | |
|---|---|
| Химическое соединение | |
| Брутто-формула | C58H95N15O15 |
| Молярная масса | 1242 г/Моль |
| CAS | 1613225-53-8 |
| PubChem | 86341926 |
| Состав | |
Биосинтез
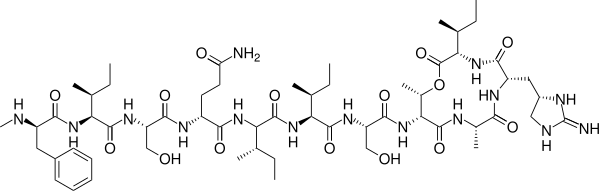
Теиксобактин состоит из 11 аминокислотных остатков, представляя собой макроциклический депсипептид, по гипотезе его первооткрывателей синтезируется в грамотрицательной бактерии Eleftheria terrae (англ.) нерибосомными пептидными синтетазами Txo1 и Txo2[2]. Пептид имеет несколько необычных особенностей, в том числе четыре D-аминокислоты, метилированный фенилаланин и не-протеиногенную аминокислоту эндурацидидин. Txo1 и Txo2 вместе состоят из 11 модулей, а каждый модуль, как полагают, последовательно добавляет одну аминокислоту к растущей пептидной цепи. Первый модуль имеет домен метилтрансферазы, который метилирует N-концевой фенилаланин. Замыкание кольца между треонином и последним изолейцином катализируется двумя С-концевыми тиоэстеразными доменами Txo2, образуя лактон[2].
Механизм действия
Теиксобактин является ингибитором синтеза клеточной стенки, действуя прежде всего за счет связывания с Lipid II (англ.), липидной молекулой, которая является предшественником пептидогликана. Это аналогично действию антибиотика ванкомицина. Связывание теиксобактина с предшественниками липидов ингибирует продукцию слоя пептидогликанов, что приводит к лизису уязвимых бактерий[2].