Преобразование энергии в фазовых переходах
Изменение энергии в фазовых переходах
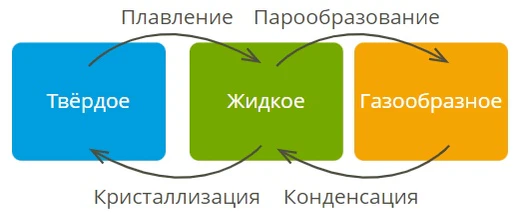
Все вещества могут находиться в трёх основных агрегатных состояниях: газообразном, жидком и твёрдом. Они могут переходить из одного состояния в другое при изменении внешних условий (температуры, давления), что называется фазовыми переходами.
Фа́зовый перехо́д —— это изменение состояния вещества при изменении внешних условий, сопровождающееся скачкообразным изменением его физических свойств.
Существуют различные фазовые переходы, такие как плавление и кристаллизация, парообразование и конденсация. Переход вещества из одной фазы в другую при постоянном давлении происходит при строго определённой температуре. Внутренняя энергия при фазовых переходах изменяется.
Для плавления вещества необходимо передать ему определённое количество теплоты. При нагревании твёрдого вещества до температуры плавления подводимая энергия затрачивается на увеличение скорости движения его частиц. Температура и внутренняя энергия продолжают расти при нагревании до точки плавления. При дальнейшем нагревании в процессе плавления подводимая энергия используется для преодоления сил притяжения между частицами. Это связано с увеличением расстояния между частицами при переходе из твердого состояния в жидкое. Скорость движения частиц при этом не меняется, поэтому температура остаётся постоянной.
Внутренняя энергия увеличивается за счет увеличения потенциальной энергии взаимодействия частиц, но кинетическая энергия частиц остаётся неизменной. Вещество в жидком состоянии имеет большую внутреннюю энергию по сравнению с твёрдым.
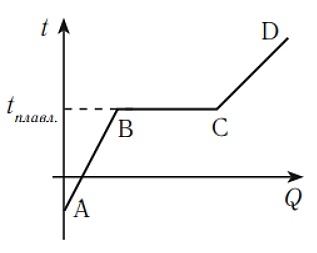
График зависимости температуры кристаллического тела от подведённого количества теплоты может быть представлен следующим образом:
Обратный переход вещества из жидкого состяние в твёрдое называется кристаллизацией. Он начинается при понижении температуры жидкости до температуры плавления. При кристаллизации выделяется количество теплоты, равное поглощаемому при плавлении. В процессе кристаллизации температура остаётся постоянной. Происходит восстановление межмолекулярных связей и кристаллической решётки.
Для вызывания процесса кипения к жидкости необходимо обеспечить подачу тепла. При нагревании температура жидкости повышается до точки кипения, а её внутренняя энергия увеличивается за счёт повышения скорости движения молекул.
Во время кипения температура жидкости остается неизменной, а внутренняя энергия продолжает возрастать благодаря увеличению потенциальной энергии взаимодействия частицам, расстояние между которыми увеличивается. При этом скорость, а следовательно, и кинетическая энергия молекул остаются постоянными.
При конденсации внутренняя энергия молекул пара уменьшается, поскольку уменьшается потенциальная энергия, кинетическая энергия остаётся постоянной и в этом случае.
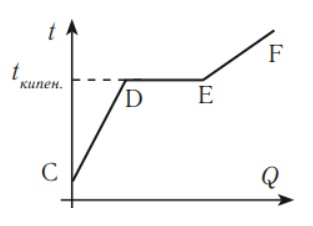
График зависимости температуры жидкости от полученного или отданного количества теплоты имеет следующий вид:
Комментарии
1. Более подробные сведения об изменении энергии в фазовых переходах (как и рассмотрение других фазовых переходов) выходят за рамки школьного курса физики.