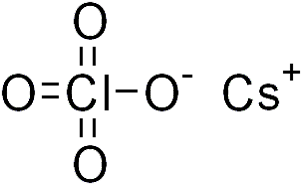Перхлорат цезия
Перхлорат цезия — химическое вещество, соль цезия и хлорной кислоты с формулой CsClO4.
Общие сведения
| Перхлорат цезия | |
|---|---|
| Общие | |
| Систематическое наименование |
Перхлорат цезия |
| Традиционные названия | Хлорнокислый цезий |
| Хим. формула | CsClO4[1] |
| Физические свойства | |
| Состояние | бесцветные кристаллы |
| Молярная масса | 232,36 г/моль |
| Плотность | 3,307 г/см³ |
| Термические свойства | |
| Температура | |
| • плавления | 250 °C |
| Энтальпия | |
| • образования | -437,2 кДж/моль |
| Химические свойства | |
| Растворимость | |
| • в воде | 0,80; 1.79425; 28.5799; |
| • в диэтиловый эфир | нерастворим |
| • в ацетон | 0.15 г/100 мл |
| • в этанол 50% | 1,522 (40°C) |
| Оптические свойства | |
| Показатель преломления | 1.4887 |
| Классификация | |
| Рег. номер CAS | 13454-84-7 |
| 3D model (JSmol) | Интерактивная схема |
| PubChem | 123309 |
| CompTox Dashboard EPA | DTXSID50884610 |
| Рег. номер EINECS | 236-643-0 |
| SMILES | |
| InChI | |
| ChemSpider | 109912 |
| ECHA InfoCard | 100.033.298 |
Общие сведения
Белые ромбические гигроскопичные кристаллы. [2]
Перхлорат цезия наименее растворим как среди перхлоратов щелочных металлов (т.е. Rb, K, Li, Na), так и среди солей цезия. Это свойство, которые может быть использовано в целях сепарации и даже быть полезным для гравиметрического анализа. Низкая растворимость перхлората цезия сыграла важную роль в охарактеризовывании франция как щелочного металла.
| Температура (°C) | 0 | 8.5 | 14 | 25 | 40 | 50 | 60 | 70 | 99 |
|---|---|---|---|---|---|---|---|---|---|
| Растворимость (г / 100 мл) | 0.8 | 0.91 | 1.91 | 1.974 | 3.694 | 5.47 | 7.30 | 9.79 | 28.57 |
Выделяется из водных растворов в виде белых блестящих кристаллов ромбической формы. При медленном охлаждении насыщенных растворов возможно получить толстые пластинки.[2]
Как и все перхлораты, CsClO4 является сильным окислителем и может бурно реагировать с восстановителями и органическими веществами, особенно при повышенных температурах. При контакте с горючими веществами может вызвать возгорание.[4]