Опыты Резерфорда по рассеянию альфа-частиц
О́пыты Резерфо́рда по рассе́янию а́льфа-части́ц — серия экспериментов, проведённых в 1909—1913 годах под руководством Эрнеста Резерфорда с участием Ханса Гейгера и Эрнеста Марсдена. Эти опыты привели к созданию планетарной модели атома, согласно которой атом имеет небольшое положительно заряженное атомное ядро, вокруг которого движутся электроны[1].
Предпосылки
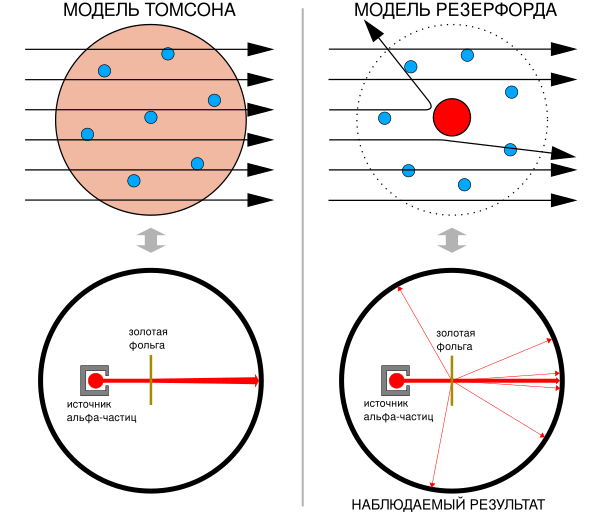
До опытов Резерфорда преобладала модель Томсона, в которой атом представлялся в виде равномерно заряженной положительной сферы с вкраплёнными в неё электронами. Согласно этой модели, альфа-частицы должны были проходить через атом без значительного отклонения[2].
Эксперименты Гейгера и Марсдена обнаружили, что небольшая часть альфа-частиц отклоняется на большие углы, вплоть до обратного направления. Это противоречило модели Томсона и указывало на наличие в атоме малого по размеру, но сильно заряженного центра.
Эксперимент
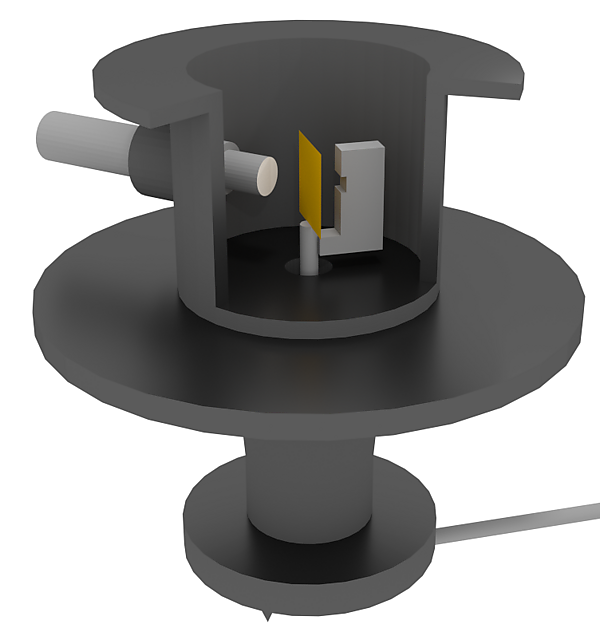
Альфа-частицы, испускаемые радиоактивным источником, направлялись на тонкую металлическую фольгу, обычно выполненную из золота. Вокруг фольги располагался экран из сульфида цинка, на котором при попадании альфа-частиц возникали вспышки света. Микроскоп, перемещаемый по кругу вокруг мишени, позволял наблюдать и подсчитывать количество альфа-частиц, рассеянных на различные углы.
В большинстве случаев альфа-частицы проходили через фольгу без отклонений или с малыми отклонениями, что соответствовало ожиданиям. Однако некоторые частицы отклонялись на большие углы, а некоторые — почти на 180°, что было неожиданно и противоречило модели Томсона.
Интерпретация и выводы
Для объяснения результатов Резерфорд предложил новую модель атома, основанную на следующих положениях:
- Почти вся масса и весь положительный заряд атома сосредоточены в центре — в ядре, радиус которого намного меньше радиуса самого атома;
- Электроны движутся вокруг ядра, подобно планетам вокруг Солнца.
Эта модель объясняла большие углы рассеяния альфа-частиц за счёт их взаимодействия с сильным электрическим полем ядра.
Резерфорд вывел формулу для количества альфа-частиц , рассеиваемых на угол :
где:
- N₀ — общее число падающих частиц,
- z — заряд альфа-частицы,
- Z — заряд ядра,
- e — элементарный заряд,
- ε₀ — электрическая постоянная,
- E — кинетическая энергия альфа-частицы.
Эта формула проверялась экспериментально и показала зависимость рассеяния от заряда ядра и энергии частиц.
Значение опытов
Опыты Резерфорда были революционными:
- Опровергли модель Томсона и продемонстрировали существование атомного ядра;
- Заложили основу для развития ядерной физики;
- Привели к пониманию структуры атома и роли ядра и электронов[3].
Заключение
Опыты Резерфорда по рассеянию альфа-частиц показали, что атом имеет сложную структуру с компактным ядром, что стало важнейшим открытием в физике. Планетарная модель атома Резерфорда стала фундаментом для дальнейшего развития квантовой теории и современной физики.
Примечания
Литература
- Айзенберг И. М., Грайнер В. Микроскопическая теория ядра. — Москва : Атомиздат, 1976.
- Бор О., Моттельсон Б. Структура атомного ядра. — Москва : Мир, 1971—1977.
- Соловьев В. Г. Теория атомного ядра : ядерные модели. — Москва : Энергоиздат, 1981.
- Сивухин Д. В. Общий курс физики. Т. 5. Ядерная физика. — Москва : Физматлит, 2014.