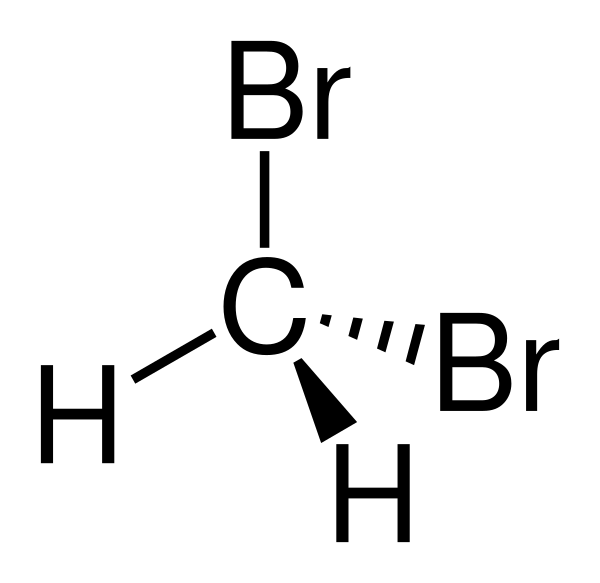
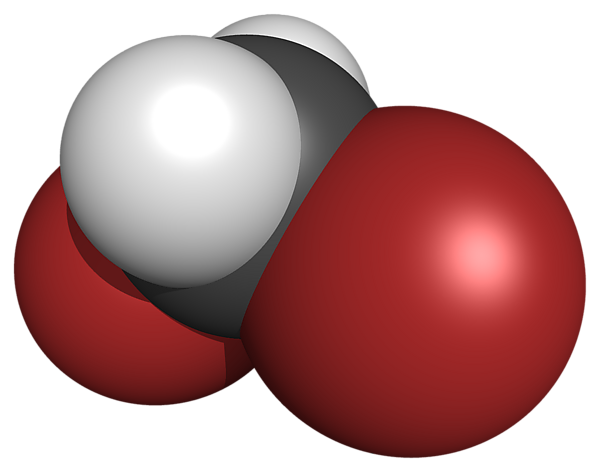
Дибромметан
Дибромметан[1] — химическое соединение является дважды замещённым представителем ряда бромметанов с бромметаном, дибромметаном, трибромметаном и тетрабромметаном.
Общие сведения
| Дибромметан | |
|---|---|
| Общие | |
| Систематическое наименование |
Дибромметан |
| Хим. формула | CH2Br2 |
| Физические свойства | |
| Состояние | жидкость |
| Молярная масса | 173,83 г/моль |
| Плотность | 2,49 г/см³ |
| Термические свойства | |
| Температура | |
| • плавления | -52 °C |
| • кипения | 97 °C |
| Классификация | |
| Рег. номер CAS | 74-95-3 |
| 3D model (JSmol) | Интерактивная схема |
| PubChem | 3024 |
| UNII | V69B659W01 |
| CompTox Dashboard EPA | DTXSID4021557 |
| Рег. номер EINECS | 200-824-2 |
| SMILES | |
| InChI | |
| RTECS | PA7350000 |
| ChEBI | 47077 |
| Номер ООН | 2664 |
| ChemSpider | 2916 |
| ECHA InfoCard | 100.000.750 |
| Безопасность | |
| Пиктограммы СГС |
|
| NFPA 704 | |
Использование
Дибромметан является промежуточным продуктом при производстве гербицидов и пестицидов.[2] Он также используется в низких концентрациях в галогенных лампах.[3]
Производство
Промышленное производство дибромметана происходит из дихлорметана путём обмена галогенов с использованием брома и алюминия.
- и
или с помощью бромистого водорода в присутствии хлорида алюминия
- и
- ,
Оба синтеза протекают через промежуточный продукт бромхлорметан. Выход обоих продуктов можно регулировать с помощью стехиометрии исходных материалов.
Как и дииодметан, дибромметан можно получить путём взаимодействия бромоформа с арсенитом натрия и гидроксидом натрия.
Другой способ получения — это реакция дииодметана с бромом.
Литература
- F. Laturnus: Образование и высвобождение галогенированных углеводородов с короткой цепью макроводорослями полярных регионов. В кн.: Отчёты о полярных исследованиях. Институт полярных и морских исследований Альфреда Вегенера, 1993, 132, стр. 188, ISSN 0176-5027.
- Ханс Петер Латша, Гельмут Альфонс Кляйн: Inorganische Chemie . Springer DE, 2002, ISBN 3-540-42938-7, стр. 408
- Majer, V .; Свобода, В.: Энтальпии испарения органических соединений: критический обзор и сбор данных , Научные публикации Блэквелла, Оксфорд, 1985, 300.
- Стулл Д. Р.: Давление паров чистых веществ и органических соединений в Индии. Eng. Chem 39 (1947) 517—540,. doi: 10.1021 / ie50448a022
Ссылки
- Podsiadlo M.; Dziubek K.; Szafranski M.; Katrusiak A. (December 2006). “Molecular interactions in crystalline dibromomethane and diiodomethane, and the stabilities of their high-pressure and low-temperature phases”. Acta Crystallogr. B. 62 (6): 1090–1098(9). DOI:10.1107/S0108768106034963. PMID 17108664. Дата обращения 2007-06-29.



![{\displaystyle {\ce {CH_2Cl_2 + HBr ->[AlCl_3] CH_2BrCl + HCl}}}](https://ru.ruwiki.ru/api/rest_v1/media/math/render/svg/da76c804f4c98712d74b6d2636b9a8c63ced0db9)
![{\displaystyle {\ce {CH_2BrCl + HBr ->[AlCl_3] CH_2Br_2 + HCl}}}](https://ru.ruwiki.ru/api/rest_v1/media/math/render/svg/6948282841bcb30b81b4d6b2401225c8f55c2cce)