Графическое представление изопроцессов на pV-, pT- и VT- диаграммах
Графическое представление изопроцессов на pV-, pT- и VT-диаграммах
Изопроцессы — это термодинамические процессы, проходящие при постоянной массе газа и неизменном значении одного из параметров состояния: температуры (), давления () или объёма (). К изопроцессам относятся:
- Изотермический процесс — процесс при постоянной температуре ().
- Изобарный процесс — процесс при постоянном давлении ().
- Изохорный процесс — процесс при постоянном объёме ().
В изотермическом процессе температура газа остаётся постоянной. Для идеального газа данный процесс описывается законом Бойля — Мариотта:
Это означает, что произведение давления на объём неизменно. При изменении состояния газа:
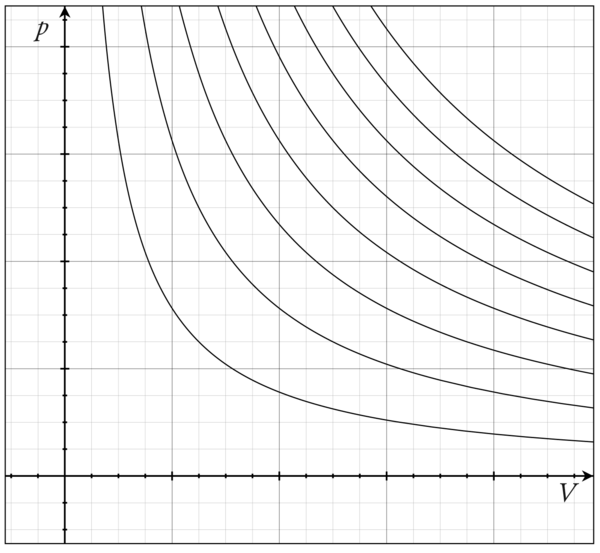
Графически изотермический процесс на pV-диаграмме представлен гиперболой — изотермой. При увеличении объёма давление уменьшается и наоборот.
В изобарном процессе давление газа остаётся постоянным. Он описывается законом Гей-Люссака:
Это означает, что объём прямо пропорционален абсолютной температуре. При переходе из одного состояния в другое:
На VT-диаграмме изобарный процесс отображается прямой линией — изобарой, проходящей через начало координат.
В изохорном процессе объём газа остаётся постоянным. Он описывается законом Шарля:
Это показывает, что давление прямо пропорционально абсолютной температуре. При изменении состояния газа:
Изохорный процесс на pT-диаграмме представлен прямой линией — изохорой, проходящей через начало координат.
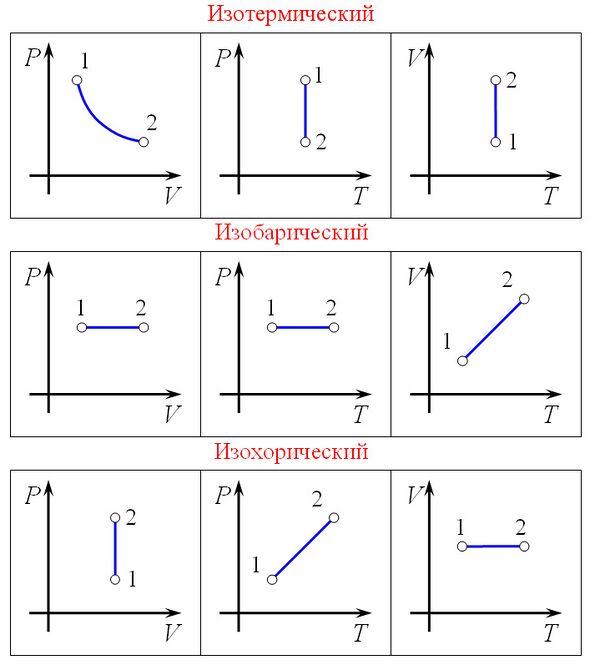
Изопроцессы можно представить на различных термодинамических диаграммах:
- На pV-диаграмме:
- Изотермы — гиперболы. - Изобары — горизонтальные прямые (). - Изохоры — вертикальные прямые ().
- На pT-диаграмме:
- Изохоры — прямые, проходящие через начало координат. - Изобары — горизонтальные прямые. - Изотермы — горизонтальные линии.
- На VT-диаграмме:
- Изобары — прямые, проходящие через начало координат. - Изохоры — вертикальные прямые. - Изотермы — горизонтальные прямые.
Графическое представление изопроцессов позволяет наглядно изучать поведение идеального газа и взаимосвязь между его параметрами.
Объединяя законы Бойля — Мариотта, Гей-Люссака и Шарля, получают объединённое уравнение состояния идеального газа:
При переходе из одного состояния в другое:
Это уравнение описывает поведение идеального газа при изменении давления, объёма и температуры, учитывая, что количество вещества остаётся постоянным.
Изопроцессы играют ключевую роль в понимании термодинамики идеального газа. Графическое представление этих процессов на pV-, pT- и VT-диаграммах предоставляет наглядное понимание взаимосвязи между параметрами состояния газа и позволяет предсказывать его поведение при различных термодинамических изменениях.