Хромат бария
| Хромат бария | |
|---|---|
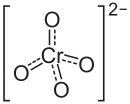 | |
| Общие | |
| Систематическое наименование |
Хромат бария |
| Хим. формула | BaCrO4 |
| Физические свойства | |
| Состояние | твердый |
| Молярная масса | 253,37 г/моль |
| Плотность | 4,5 г/см³ |
| Термические свойства | |
| Температура | |
| • плавления | 1380 °C |
| Энтальпия | |
| • образования | -1366,8 кДж/моль |
| Химические свойства | |
| Растворимость | |
| • в воде | (при 20 °C) 0,00028 г/100 мл |
| Классификация | |
| Рег. номер CAS | 10294-40-3 |
| 3D model (JSmol) | Интерактивная схема |
| PubChem | 25136 |
| UNII | 7D7O9CF0IX |
| CompTox Dashboard EPA | DTXSID1051517 |
| Рег. номер EINECS | 233-660-5 |
| SMILES | |
| InChI | |
| RTECS | CQ876000 |
| ChemSpider | 23481 |
| ECHA InfoCard | 100.030.587 |
| Безопасность | |
| Предельная концентрация | 0,01 мг/м³ |
| Токсичность | Класс опасности 1 |
| Пиктограммы ECB |
|
| NFPA 704 | |
| Приведены данные для стандартных условий (25 °C, 100 кПа), если не указано иное. | |
Хромат бария — бариевая соль хромовой кислоты, имеющая химическую формулу BaCrO4.
Физические и химические свойства
Хромат бария представляет собой ярко-жёлтое кристаллическое вещество плохо растворимое в воде (ПР=1,2⋅10−10[1]). Низкая растворимость этого соединения используется в аналитической практике для отделения и определения солей бария.
В растворах сильных неорганических кислот растворяется с образованием бихромата:
Плохо растворим в уксусной кислоте, что используется для отделения бария от ионов стронция [1].
При прокаливании в смеси с Ba(OH)2 и присутствии азида натрия превращается в хромат(V) бария. При этом выделяется кислород и вода:
Получение
Взаимодействием растворов Ba(OH)2 или BaS с хроматом натрия или калия:
Окисление гидроксида хрома(III) в водном растворе гидроксида бария с помощью хлора, брома, гипохлорита натрия, пероксида водорода или оксида свинца(IV):
Взаимодействие дихромата калия с раствором хлорида бария:
За счёт образования в данной реакции дихромовой кислоты, добиться полного осаждения хрома невозможно. Чтобы количественно осадить весь хром в растворе, в реакционную смесь добавляют ацетат натрия. Дихромовая кислота сильнее уксусной, а потому вытесняет её из солей:
Токсичность
Применение
- Пигмент («баритовый жёлтый»[2][3] или «жёлтый ультрамарин»[4][5]) для керамики, фарфора, красок.
- Входит в состав некоторых пиротехнических композиций.
- Компонент безопасных спичек.
- Ингибитор коррозии.
- Для изготовления воспламеняющих составов.
- Один из возможных реагентов для осаждения радия из кислых урановых растворов[6].
Литература
- Неорганическая химия / под ред. Ю.Д. Третьякова. — М.: Академия, 2007. — Т. 3. — 352 с.






