Химическое строение органических соединений и их структурные особенности
Хими́ческое строе́ние органи́ческих соедине́ний — порядок соединения атомов в молекуле и их взаимное расположение в пространстве. В органических соединениях атомы соединены друг с другом согласно их валентности.
Основная часть
Большинство органических соединений имеют молекулярное строение. Атомы в веществах с молекулярным типом строения всегда образуют только ковалентные связи друг с другом, что наблюдается и в случае органических соединений.
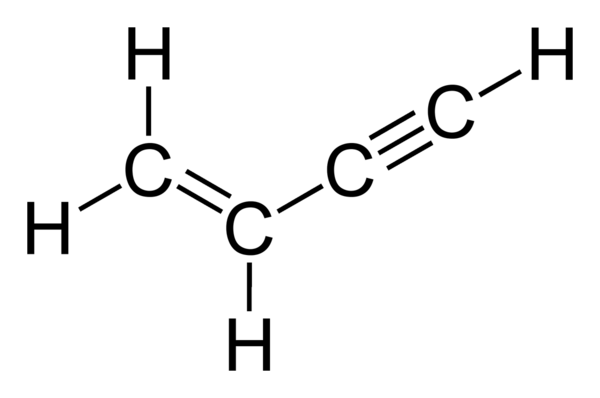
Ковалентным называется такой вид связи между атомами, который реализуется за счёт того, что атомы обобществляют часть своих внешних электронов с целью приобретения электронной конфигурации благородного газа. По количеству обобществлённых электронных пар ковалентные связи в органических веществах можно разделить на одинарные, двойные и тройные. Обозначаются данные типы связей в графической формуле одной, двумя или тремя чертами. Кратность связи приводит к уменьшении её длины, так одинарная С-С связь имеет длину 0,154 нм, двойная С=С связь – 0,134 нм, тройная С≡С связь – 0,120 нм[1].
Гибридиза́ция орбита́лей — гипотетический процесс смешения различных атомных орбиталей (s, p, d, f) центрального атома многоатомной молекулы с возникновением одинаковых орбиталей, эквивалентных по своим правилам. Угол между гибридными орбиталями при sp3-гибридизации равен 109.5°, при sp2 — 120°, при sp — 180°.
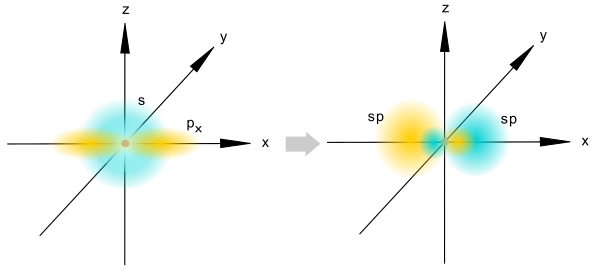
При sp - гибридизации s - орбиталь углерода в возбуждённом состоянии смешивается только с одной из трёх 2p - орбиталей. Это называется sp - гибридизацией, потому что две орбитали (одна s и одна p) смешаны. Получающиеся две sp - гибридные орбитали затем располагаются в линейной геометрии (180°), а две негибридизованные 2p - орбитали располагаются под углом 90°. В ацетилене - C2H2 два атома углерода образуют сигма - связь, перекрывая sp - орбитали. Один водород связывается с каждым атомом углерода, перекрывая его орбиталь с другой орбиталью. Две p - орбитали каждого углерода перекрываются, образуя две π-связи.
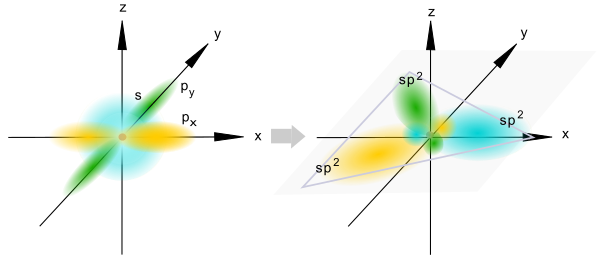
Данный вид гибридизации происходит при смешивании одной s- и двух p-орбиталей. Образуются три гибридные орбитали с осями, расположенными в одной плоскости и направленными к вершинам треугольника под углом 120°. Негибридная p-атомная орбиталь перпендикулярна плоскости и, как правило, участвует в образовании π-связей.
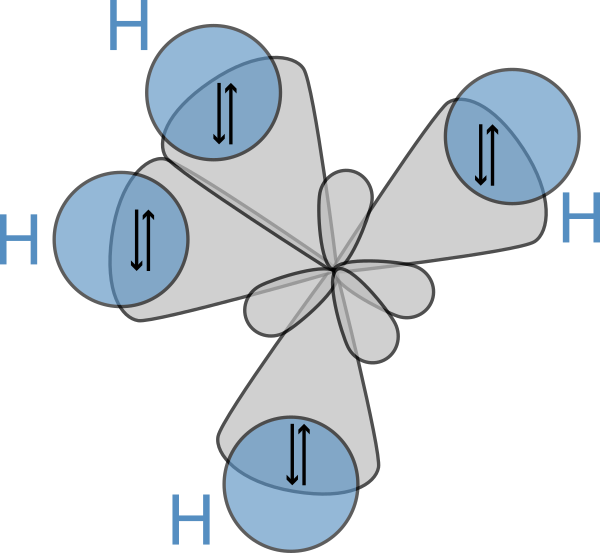
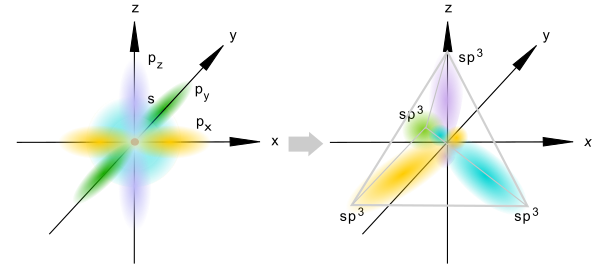
Данный вид гибридизации происходит при смешивании одной s- и трех p-орбиталей, образуя четыре равноценные по форме и энергии sp3-гибридные орбитали.
Оси sp3-гибридных орбиталей направлены к вершинам тетраэдра, тогда как ядро центрального атома расположено в центре описанной сферы этого тетраэдра. Угол между любыми двумя осями приближённо равен 109°28', что соответствует наименьшей энергии отталкивания электронов. Также sp3-орбитали могут образовывать четыре σ-связи с другими атомами или заполняться неподелёнными парами электронов. Такое состояние характерно для атомов углерода в насыщенных углеводородах и соответственно в алкильных радикалах и их производных.
Под термином радикал, чаще всего подразумевают углеводородный радикал, являющийся остатком молекулы какого-либо углеводорода без одного атома водорода. Название углеводородного радикала формируется, исходя из названия соответствующего ему углеводорода заменой суффикса –ан на суффикс –ил (метил, этил, пропил)[2].
Функциональная группа
Функциона́льная гру́ппа — структурный фрагмент органической или неорганической молекулы (некоторая группа атомов), определяющий её химические свойства. Для органических соединений старшая функциональная группа соединения является критерием его отнесения к тому или иному классу.
Функциональные группы, входящие в состав различных молекул, обычно ведут себя одинаково в одной и той же химической реакции, хотя их химическая активность может быть различной.
Известно более 100 функциональных групп.
- Функциональные группы, содержащие атом кислорода:
- гидроксильная –ОН,
- карбонильная >С=O,
- карбоксильная –COOH,
- алкоксильная –OR (типа –ОСН3) и др.
- Функциональные группы, содержащие атом азота:
- аминогруппа –NH2,
- нитрогруппа –NO2,
- нитрозогруппа –NO,
- нитрильная группа или цианогруппа –CN,
- гидразинная –NHNH2,
- амидная –CONH2 и др.
- Функциональные группы, содержащие атом серы:
- тиольная (сульфгидрильная, меркапто-) –SH,
- сульфидная >S,
- дисульфидная –S–S–,
- сульфоксидная >S=O,
- сульфонная >SO2 и др.
- Функциональные группы, содержащие ненасыщенные углерод-углеродные связи:
- двойные и тройные связи (в том числе сопряжённые диеновые системы) –С=С–, –С≡С–,
- ароматические фрагменты –С6H5 и др.
- Функциональные группы, содержащие прочие атомы:
Молекулы, в состав которых входит больше чем одна функциональная группа называются полифункциональными.
При построении названия органического соединения, согласно номенклатуре ИЮПАК, отталкиваются от наличия в данном соединении функциональных групп[3].
Заключение
Знание строения органических соединений и типы гибридизаций помогает понять как и в какие реакции могут вступать соединения, а также позволяет выяснить как атомы видоизменяют свои орбитали при образовании соединений.
Примечания
- ↑ Строение органических соединений и электронные эффекты. orgchem.tsu.ru. Дата обращения: 29 марта 2025.
- ↑ Обучение / Интернет-лицей | ТПУ (англ.). il.tpu.ru. Дата обращения: 29 марта 2025.
- ↑ Бокий, Георгий Борисович - Введение в номенклатуру ИЮПАК : как назвать химическое соединение - Search RSL (рус.). search.rsl.ru. Дата обращения: 29 марта 2025.
Литература
- Кузнецова Н. Е., Гара Н. Н., Титова И. М. Химия. 10 класс. Углубленный уровень. — 2019. — 409 с.
- Габриелян О. С., Остроумов И. Г., Пономарев С. Ю. Химия. 10 класс. Углубленный уровень. — "Российский учебник", 2019. — 364 с.
- Еремин В. В., Кузьменко Н. Е., Теренин В. И., Дроздов А. А., Лунин В. В. Химия. 10 класс. Углубленный уровень. — "Дрофа", 2019. — 409 с.
- Еремин В. В., Кузьменко Н. Е., Дроздов А. А., Лунин В. В. Химия. 11 класс. Углубленный уровень. — "Российский учебник", 2019. — 409 с.
- Габриелян О. С., Лысова Г. Г. Химия. 11 класс. Углубленный уровень. — "Дрофа", 2019. — 394 с.
Категории
| Правообладателем данного материала является АНО «Интернет-энциклопедия «РУВИКИ». Использование данного материала на других сайтах возможно только с согласия АНО «Интернет-энциклопедия «РУВИКИ». |