Химические свойства белков
Химические свойства белков — это совокупность характеристик, определяющих поведение белков в химических реакциях, их взаимодействие с окружающей средой, растворимость и стабильность структуры.
Амфотерность
Белки обладают свойством амфотерности, то есть могут проявлять как кислотные, так и основные свойства в зависимости от условий среды. Это обусловлено наличием в их составе функциональных групп:
- Кислотные группы — карбоксильные остатки () боковых цепей кислых аминокислот (аспарагиновая и глутаминовая кислоты).
- Основные группы — аминогруппы () боковых цепей основных аминокислот (лизин, аргинин, гистидин).
Каждый белок характеризуется изоэлектрической точкой (pI) — значением pH, при котором суммарный электрический заряд его молекул равен нулю (). В изоэлектрической точке белки минимально растворимы и не перемещаются в электрическом поле при электрофорезе. Значение pI зависит от соотношения кислых и основных аминокислот:
- Белки с преобладанием кислых аминокислот имеют pI в кислой области (5,5—7,0).
- Белки с преобладанием основных аминокислот имеют pI в щелочной области (выше 7,0).
Растворимость
Белки различаются по степени растворимости в воде:
- Растворимые белки (альбумины) присутствуют в крови и молоке.
- Нерастворимые белки (склеропротеины) входят в состав волос, перьев, шёлка и паутины (например, кератин и фиброин).
Растворимость белков зависит от:
- Природы белка (гидрофильные или гидрофобные участки).
- Внешних факторов: pH, ионной силы раствора, природы растворителя.
Гидрофильные белки хорошо взаимодействуют с водой и обычно располагаются в цитоплазме клеток. Гидрофобные белки содержат участки, отталкивающие воду, что характерно для интегральных мембранных белков, взаимодействующих с липидами клеточных мембран.
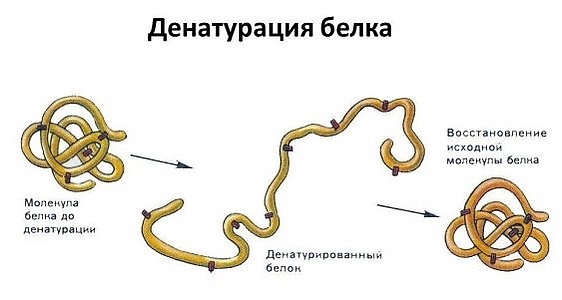
Денатурация
Денатурация белка — процесс изменения природной структуры белка (вторичной, третичной или четвертичной), приводящий к потере биологической активности. Причины денатурации могут быть различными:
- Физические воздействия: высокая температура, ультрафиолетовое излучение, ультразвук.
- Химические агенты: кислоты, щёлочи, соли тяжёлых металлов, органические растворители.
- Механические воздействия: сильное встряхивание, перемешивание.
Денатурация может быть:
- Обратимой — структура белка восстанавливается при устранении денатурирующего фактора.
- Необратимой — структура белка не восстанавливается, и он не может выполнять свои функции.
Пример необратимой денатурации — сваренное куриное яйцо: под действием высокой температуры растворимый белок овальбумин теряет природную структуру и образует плотную нерастворимую массу.
Заключение
Химические свойства белков обусловлены их амфотерной природой, разнообразным аминокислотным составом и структурной организацией. Понимание этих свойств важно для изучения биологических процессов в организме, разработки лекарственных препаратов и технологий в пищевой промышленности.
Литература
- Кузнецова Н. Е., Гара Н. Н., Титова И. М. Химия. 10 класс. Углубленный уровень. — 2019. — 409 с.
- Габриелян О. С., Остроумов И. Г., Пономарев С. Ю. Химия. 10 класс. Углубленный уровень. — "Российский учебник", 2019. — 364 с.
- Еремин В. В., Кузьменко Н. Е., Теренин В. И., Дроздов А. А., Лунин В. В. Химия. 10 класс. Углубленный уровень. — "Дрофа", 2019. — 409 с.
- Еремин В. В., Кузьменко Н. Е., Дроздов А. А., Лунин В. В. Химия. 11 класс. Углубленный уровень. — "Российский учебник", 2019. — 409 с.
- Габриелян О. С., Лысова Г. Г. Химия. 11 класс. Углубленный уровень. — "Дрофа", 2019. — 394 с.