Физические и химические свойства сероводорода
Сероводород (сернистый водород, сульфид водорода) — бинарное химическое соединение водорода и серы с формулой H₂S. Это бесцветный газ со сладковатым вкусом и характерным неприятным запахом тухлых яиц. Сероводород плохо растворим в воде, хорошо растворим в этаноле, огнеопасен и очень токсичен.
Физические свойства
- Молекулярная структура: молекула сероводорода имеет изогнутую форму с углом между связями около 92°, она полярна (дипольный момент μ = 0,102 Д).
- Термическая устойчивость: стабилен до температуры около 400 °C, при более высокой температуре разлагается на серу и водород.
- Растворимость: растворяется в воде с образованием слабой сероводородной кислоты; хорошо растворим в этаноле.
- Жидкий сероводород: не образует водородных связей, поэтому не сжижается при обычных условиях.
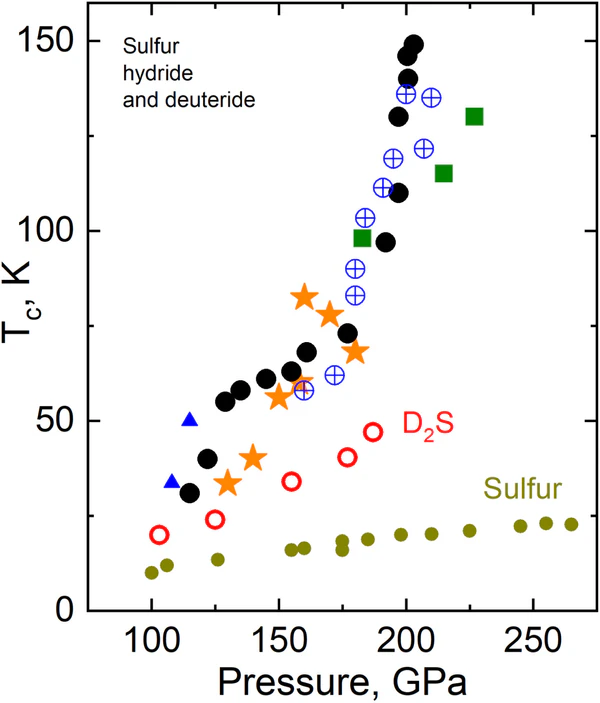
- Сверхпроводимость: при высоких давлениях (около 150 ГПа) переходит в сверхпроводящее состояние с критической температурой до 203 К (−70 °C).
Химические свойства
- Кислотные свойства: сероводородная кислота является очень слабой кислотой:
* Ионизация:
* Константа диссоциации: Kₐ = 6,9 × 10⁻⁷; pKₐ = 6,89.
- Реакции с щелочами:
* Образование сульфидов: * * Образование гидросульфидов: *
- Восстановительные свойства: сероводород является сильным восстановителем.
* Горение в кислороде: * * При недостатке кислорода: *
- Реакции с окислителями:
* С диоксидом серы: * * С перекисью водорода: *
- Качественная реакция: взаимодействие с солями свинца с образованием чёрного осадка сульфида свинца:
*
Получение
- Действие кислот на сульфиды металлов:
*
- Гидролиз сульфида алюминия:
*
Применение
- Химическая промышленность: используется для получения элементной серы, серной кислоты и сульфидов.
- Аналитическая химия: применяется для обнаружения и осаждения ионов тяжёлых металлов.
- Органический синтез: используется для синтеза серосодержащих органических соединений, таких как тиофен и меркаптаны.
Токсичность
Сероводород — высокотоксичный газ. При низких концентрациях вызывает головную боль, тошноту, головокружение. В высоких концентрациях может привести к потере сознания, коме, отёку лёгких и смерти. Обладает раздражающим действием на слизистые оболочки и дыхательные пути.
Заключение
Сероводород — важное химическое соединение с характерными физическими и химическими свойствами. Его способность вступать в разнообразные реакции делает его ценным в промышленности и лабораторной практике. Однако высокая токсичность требует строгого соблюдения мер безопасности при работе с этим веществом.
Литература
- Габриелян О. С., Остроумов И. Г., Ахлебинин А. К. Химия. 7 класс.. — "Дрофа", 2019. — 161 с.
- Габриелян О. С., Остроумов И. Г., Сладков С.А. Химия. 8 класс. Базовый уровень.. — «Просвещение», 2024. — 176 с.
- Габриелян О. С. Химия. 8 класс.. — "Дрофа", 2019. — 284 с.
- Габриелян О. С., Остроумов И. Г., Сладков С.А. Химия. 9 класс.. — «Просвещение», 2023. — 224 с.
- Ерёмин В. В., Кузьменко Н. Е., Дроздов А. А. и др. Химия. 9 класс.. — 2022. — 291 с.