Физические и химические свойства азота
Азот — это химический элемент с символом N и атомным номером 7, представляющий собой бесцветный, без запаха, малорастворимый в воде газ, составляющий около 78 % объёма земной атмосферы.
Физические свойства
- Бесцветный газ без запаха при нормальных условиях.
- Малорастворим в воде: 2,3 мл/100 г при 0 °C, снижается с повышением температуры.
- Плотность: 1,2506 кг/м³ при нормальных условиях.
- Жидкий азот:
* Температура кипения: −195,8 °C. * Бесцветная, подвижная жидкость с плотностью 808 кг/м³. * При контакте с воздухом поглощает кислород.
- Твёрдый азот:
* Температура замерзания: −209,86 °C. * Имеет три полиморфные модификации: * β-N₂: гексагональная решётка при 36,61—63,29 K. * α-N₂: кубическая решётка при температурах ниже 36,61 K. * γ-N₂: гексагональная фаза под давлением более 3500 атм и температуре ниже 83 K.
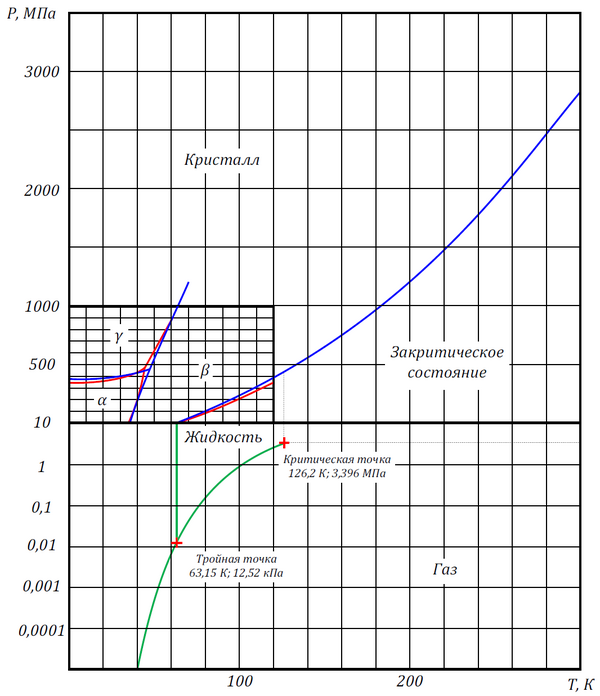
Фазовая диаграмма
Химические свойства
- Молекула азота: двухатомная N₂ с тройной связью N≡N.
* Длина связи: 0,1095 нм. * Электронная конфигурация: 1s2 2s2 2p3.
- Высокая прочность связи:
* Энергия диссоциации: ΔH°₂₉₈ = 945 кДж/моль. * Инертность: при обычных условиях слабо реагирует.
- Термическая диссоциация:
* При 3000 °C степень диссоциации всего 0,1 %. * При 5000 °C достигает нескольких процентов.
- С литием при комнатной температуре:
*
- При нагревании реагирует с:
* Магнием: * * Бором: *
- С водородом (синтез аммиака):
*
* Реакция экзотермическая, проводится при повышенных температуре и давлении с катализатором.
- В электрическом разряде образует оксид азота(II):
*
- Процесс Габера (синтез аммиака):
* Ключевой метод получения соединений азота. * Используется железный катализатор с примесями оксидов алюминия и калия. * Условия реакции: * Температура: 400—600 °C. * Давление: 10—1000 атм.
- Цианамидный метод:
* Реакция карбида кальция с азотом:
*
* Проводится при 1000 °C, экзотермическая реакция.
Заключение
Азот — инертный газ с прочной тройной связью, что определяет его физические и химические свойства. Его способность образовывать различные соединения при определённых условиях делает азот важным элементом в промышленности, особенно в производстве аммиака и удобрений. Понимание свойств азота имеет ключевое значение для технологий, связанных с химическим синтезом и переработкой материалов.
Литература
- Габриелян О. С., Остроумов И. Г., Ахлебинин А. К. Химия. 7 класс.. — "Дрофа", 2019. — 161 с.
- Габриелян О. С., Остроумов И. Г., Сладков С.А. Химия. 8 класс. Базовый уровень.. — «Просвещение», 2024. — 176 с.
- Габриелян О. С. Химия. 8 класс.. — "Дрофа", 2019. — 284 с.
- Габриелян О. С., Остроумов И. Г., Сладков С.А. Химия. 9 класс.. — «Просвещение», 2023. — 224 с.
- Ерёмин В. В., Кузьменко Н. Е., Дроздов А. А. и др. Химия. 9 класс.. — 2022. — 291 с.







![{\displaystyle N_{2}+O_{2}\leftrightarrow [{2000\ ^{\circ }{\text{C}}}]2NO-Q}](https://ru.ruwiki.ru/api/rest_v1/media/math/render/svg/93a73da5fab1ee6822954a6fdb7e5dfcfb8ee77d)
