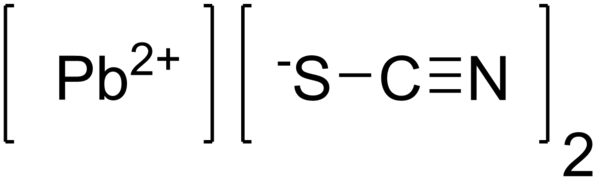Тиоцианат свинца(II)
Тиоциана́т свинца́(II) — неорганическое соединение, соль свинца и роданистоводородной кислоты с формулой Pb(SCN)2, белые кристаллы, не растворяется в воде.
Общие сведения
| Тиоцианат свинца(II) | |
|---|---|
| Общие | |
| Систематическое наименование |
Тиоцианат свинца(II) |
| Традиционные названия | Тиоциановокислый свинец; роданистый свинец; роданид свинца |
| Хим. формула | Pb(SCN)2 |
| Физические свойства | |
| Состояние | белые кристаллы |
| Молярная масса | 323,36 г/моль |
| Плотность | 3,82; 4,082; 4,1 г/см³ |
| Термические свойства | |
| Температура | |
| • разложения | 190 °C |
| Химические свойства | |
| Растворимость | |
| • в воде | 0,0520 г/100 мл |
| Классификация | |
| Рег. номер CAS | 592-87-0 |
| 3D model (JSmol) | Интерактивная схема |
| PubChem | 11616 |
| UNII | 7977FZ765Q |
| CompTox Dashboard EPA | DTXSID90890513 |
| Рег. номер EINECS | 209-774-6 |
| SMILES | |
| InChI | |
| ChemSpider | 21501026 и 11127 |
| ECHA InfoCard | 100.008.887 |
| Безопасность | |
| Предельная концентрация | 0,01 мг/м³ |
| NFPA 704 | |
Получение
- Обменная реакция холодных растворов тиоцианата калия (или тиоцианата натрия, тиоцианата аммония) и нитрата свинца(II) (или ацетата свинца(II)):
- Осадок отфильтровывают, отмывают от нитрат- или ацетат-иона и высушивают в вакуум-эксикаторе над пятиокисью фосфора в темноте.
Физические свойства
Тиоцианат свинца(II) образует белые кристаллы моноклинной сингонии, пространственная группа С 2/с, параметры ячейки a = 0,9661 нм, b = 0,6544 нм, c = 0,8253 нм, β = 92,37°, Z = 4 [1].
Не растворяется в холодной воде, р ПР = 4,7. В горячей воде растворимость несколько выше. Хорошо растворяется в воде, подкислённой соляной кислотой.
Чувствителен к воздействию света.
Химические свойства
- Растворяется в ацетоновом растворе тиоцианата калия:
- На воздухе медленно окисляется с образованием родана и диоксида свинца[2]:
Применение
- Стабилизатор горения капсюльных составов и спичек. Входит в состав инициирующих взрывчатых веществ как горючий компонент, образующий большое количество твёрдых продуктов горения[3].
- Используют для лабораторного синтеза родана (дитиоциана).
Примечания
Литература
- Справочник химика / Редкол.: Б. П. Никольский и др.. — 3-е изд., испр. — Л.: Химия, 1971. — Т. 2. — 1168 с.
- CRC Handbook of Chemistry and Physics. — 89th Edition. — Taylor and Francis Group, LLC, 2008—2009.
- Руководство по неорганическому синтезу: В 6-ти т. / Ред. Г. Брауэр. — М.: Мир, 1985. — Т. 3. — 392 с.
- Химический энциклопедический словарь / Редкол.: И. Л. Кнунянц и др.. — М.: Советская энциклопедия, 1983. — 792 с.



![{\displaystyle {\mathsf {Pb(SCN)_{2}+4KSCN\ {\xrightarrow {}}\ K_{4}[Pb(SCN)_{6}]}}}](https://ru.ruwiki.ru/api/rest_v1/media/math/render/svg/31fc2f2c7a8afcc045461d5f1bdb3fbcbd621a93)