Спектр уровней энергии атома водорода
Спектр уровней энергии атома водорода — распределение энергетических состояний электрона в атоме водорода, определяющее спектральные линии излучения и поглощения этого атома. Эти энергетические уровни дискретны и соответствуют определённым значениям энергии, которые может принимать электрон согласно законам квантовой механики.
Атом водорода состоит из протона и электрона, взаимодействующих по закону Кулона. Электрон может находиться только в определённых стационарных состояниях с фиксированной энергией — энергетических уровнях. При переходе электрона между уровнями происходит излучение или поглощение фотона с энергией, равной разности энергий этих уровней:
,
где h — постоянная Планка, ν — частота излучения, Eₙ и Eₙ' — энергии начального и конечного уровней.
Энергия уровней определяется выражением:
,
где Rₕ — постоянная Ридберга для водорода, c — скорость света, n — главное квантовое число (n = 1, 2, 3, ...).
Переходы электрона между энергетическими уровнями приводят к появлению спектральных линий, сгруппированных в серии, описываемые формулой Ридберга:
,
где λ — длина волны излучения, n' — нижний энергетический уровень (n' = 1, 2, 3, ...), n — верхний уровень (n > n' ).
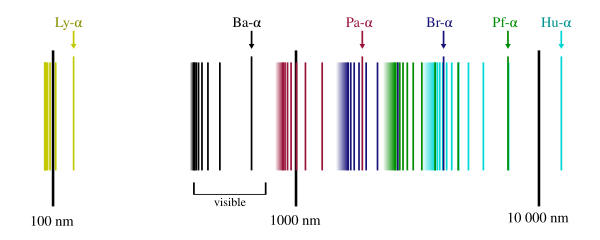
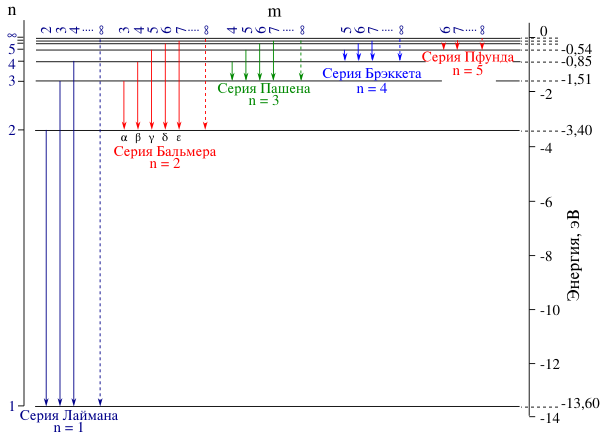
Основные серии:
- **Серия Лаймана** (n' = 1): линии в ультрафиолетовом диапазоне.
- **Серия Бальмера** (n' = 2): первые четыре линии в видимом диапазоне.
- **Серия Пашена** (n' = 3): линии в инфракрасном диапазоне.
- **Серия Брэккета** (n' = 4): линии в инфракрасном диапазоне.
- **Серия Пфунда** (n' = 5): линии в дальнем инфракрасном диапазоне.
Формула Ридберга позволяет точно определить длины волн спектральных линий:
.
Постоянная Ридберга для водорода равна:
.
Это позволяет вычислить длины волн и частоты излучения при переходах между уровнями.
Состояния электрона в атоме водорода характеризуются набором квантовых чисел:
- **Главное квантовое число** n определяет энергию уровня и размер орбитали.
- **Орбитальное квантовое число** l (от 0 до n–1) определяет форму орбитали и орбитальный угловой момент: .
- **Магнитное квантовое число** mₗ (от –l до +l) определяет проекцию углового момента на выбранную ось: .
- **Спиновое квантовое число** mₛ = ±½ характеризует собственный момент импульса (спин) электрона.
Решение уравнения Шрёдингера для атома водорода даёт волновые функции — орбитали, определяющие распределение вероятности нахождения электрона в пространстве. Волновая функция выражается через радиальную и угловые части:
,
где Rₙₗ — радиальная функция, Yₗₘ — сферические гармоники.
Из-за релятивистских и спин-орбитальных взаимодействий уровни энергии слегка смещаются (тонкая структура). Энергии уровней записываются как:
,
где α — постоянная тонкой структуры, j — полный момент электрона (j = l ± ½).
Изображения орбиталей показывают области пространства, где вероятность нахождения электрона максимальна. Форма орбиталей зависит от квантовых чисел n, l и mₗ.
Изучение спектра уровней энергии атома водорода сыграло ключевую роль в развитии квантовой механики. Модель атома водорода позволяет понять природу дискретности энергетических уровней и объяснить спектральные линии излучения. Эти принципы применимы не только к водороду, но и к более сложным атомам, что делает их фундаментальными для всей атомной физики и спектроскопии.