Общие химические свойства угольной кислоты
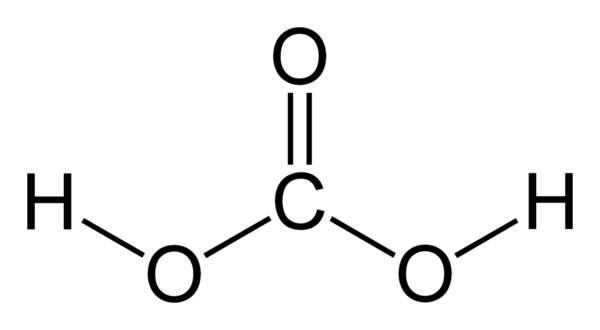
Угольная кислота — слабая двухосновная кислота формулы H₂CO₃, образуется при растворении диоксида углерода в воде.
Химические свойства
Угольная кислота существует в водных растворах в состоянии равновесия с гидратированным диоксидом углерода:
Константа равновесия при 25 °C:
Угольная кислота — слабая двухосновная кислота, которая диссоциирует в два этапа:
1. Первая ступень диссоциации:
:
Константа кислотности:
:
2. Вторая ступень диссоциации:
:
Константа кислотности:
:
Общая схема равновесий в растворе:
В насыщенном растворе CO₂ при 25 °C и давлении 760 мм рт. ст. концентрация CO₂ составляет 0,034 моль/л. pH такого раствора можно рассчитать:
Где кажущаяся константа кислотности Kₐ' учитывает равновесие между CO₂•H₂O и H₂CO₃:
Угольная кислота неустойчива и легко разлагается на воду и диоксид углерода:
Разложение ускоряется при повышении температуры или понижении давления CO₂.
Угольная кислота реагирует с основаниями, образуя карбонаты и гидрокарбонаты.
1. Реакция с избытком щёлочи (образование карбонатов):
:
2. Реакция с недостатком щёлочи (образование гидрокарбонатов):
:
3. Реакция с растворимыми основаниями:
:
4. Реакция с нерастворимыми основаниями:
:
Угольная кислота реагирует с карбонатами, образуя гидрокарбонаты:
1. С карбонатами щелочных металлов:
:
2. С нерастворимыми карбонатами:
:
Полученные гидрокарбонаты чаще растворимы в воде и могут создавать жёсткость воды.
Заключение
Угольная кислота играет важную роль в природных процессах и технологиях, связанных с CO₂. Её слабые кислотные свойства и способность образовывать карбонаты и гидрокарбонаты важны в химии, биологии и экологии. Понимание её свойств помогает объяснить процессы, происходящие в атмосфере, гидросфере и организме человека.
Литература
- Габриелян О. С., Остроумов И. Г., Ахлебинин А. К. Химия. 7 класс.. — "Дрофа", 2019. — 161 с.
- Габриелян О. С., Остроумов И. Г., Сладков С.А. Химия. 8 класс. Базовый уровень.. — «Просвещение», 2024. — 176 с.
- Габриелян О. С. Химия. 8 класс.. — "Дрофа", 2019. — 284 с.
- Габриелян О. С., Остроумов И. Г., Сладков С.А. Химия. 9 класс.. — «Просвещение», 2023. — 224 с.
- Ерёмин В. В., Кузьменко Н. Е., Дроздов А. А. и др. Химия. 9 класс.. — 2022. — 291 с.






![{\displaystyle K_{p}={\frac {\mathsf {[H_{2}CO_{3}]}}{\mathsf {[CO_{2}\cdot H_{2}O]}}}=1{,}70\cdot 10^{-3}}](https://ru.ruwiki.ru/api/rest_v1/media/math/render/svg/d37e7cded585ef31bd6c1e0bffe2059cb4c31301)

![{\displaystyle K_{a1}={\frac {\mathsf {[HCO_{3}^{-}][H_{3}O^{+}]}}{\mathsf {[H_{2}CO_{3}]}}}=2{,}5\cdot 10^{-4}}](https://ru.ruwiki.ru/api/rest_v1/media/math/render/svg/5abb210d71364cf3a029bee4f213ed8183410e22)

![{\displaystyle K_{a2}={\frac {\mathsf {[CO_{3}^{2-}][H_{3}O^{+}]}}{\mathsf {[HCO_{3}^{-}]}}}=4{,}68\cdot 10^{-11}}](https://ru.ruwiki.ru/api/rest_v1/media/math/render/svg/edeb5297f044e3154790d79a420acaf51dd141b2)


![{\displaystyle K_{a}'={\frac {\mathsf {[HCO_{3}^{-}][H_{3}O^{+}]}}{\mathsf {[CO_{2}\cdot H_{2}O]}}}=4{,}27\cdot 10^{-7}}](https://ru.ruwiki.ru/api/rest_v1/media/math/render/svg/5ffd9b1824badcda986e1714c7224bcee0e26d45)






