Насыщенные и ненасыщенные растворы, растворимость
Раствори́мость — способность вещества образовывать однородные системы — растворы — с другими веществами, где оно присутствует в виде отдельных атомов, ионов или молекул. Растворимость выражается концентрацией растворённого вещества в его насыщенном растворе.
Основные понятия
- Ненасыщенный раствор — раствор, в котором концентрация растворённого вещества меньше, чем в насыщенном растворе при данных условиях, и в который можно добавить ещё растворяемого вещества.
- Насыщенный раствор — раствор, где растворённое вещество достигло максимальной концентрации при данных условиях и больше не растворяется. Между растворённым веществом и его осадком устанавливается химическое равновесие.
- Пересыщенный раствор — раствор, содержащий больше растворённого вещества, чем в насыщенном растворе при тех же условиях. Такие растворы нестабильны; избыток вещества легко выпадает в осадок. Пересыщенные растворы получают путём охлаждения насыщенного раствора.
- Концентрированный раствор — раствор с высоким содержанием растворённого вещества.
- Разбавленный раствор — раствор с низким содержанием растворённого вещества.
Растворимость и факторы, влияющие на неё
Растворимость веществ зависит от нескольких факторов:
- Температура: для большинства твёрдых и жидких веществ растворимость увеличивается с повышением температуры. Для газов растворимость обычно уменьшается при повышении температуры.
- Давление: влияет преимущественно на растворимость газов — при увеличении давления растворимость газов в жидкостях растёт.
- Природа растворяемого вещества и растворителя: согласно правилу «подобное растворяется в подобном», полярные вещества хорошо растворяются в полярных растворителях, а неполярные — в неполярных.
- Наличие других веществ: присутствие в растворителе других растворённых веществ может изменять растворимость (эффект высаливания, изменение полярности растворителя и др.).
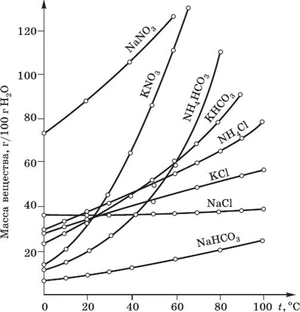
Кривые растворимости
Кривые растворимости отображают зависимость растворимости вещества от температуры. На графике показано, как при изменении температуры меняется максимальное количество растворённого вещества в насыщенном растворе[1].
Способы выражения растворимости
- Качественные характеристики: описательные термины, такие как «хорошо растворимо», «мало растворимо», «нерастворимо». Эти оценки субъективны и зависят от контекста.
- Количественные характеристики: конкретные значения растворимости, выраженные в единицах концентрации, например:
* Граммы вещества на 100 г растворителя (г/100 г). * Молярная концентрация (моль/л). * Мольная доля.
Методы измерения растворимости
- Гравиметрический метод: растворение вещества до насыщения, отделение нерастворившегося остатка и определение концентрации растворённого вещества.
- Физико-химические методы: использование инструментальных методов анализа (спектроскопия, хроматография) для определения низких концентраций веществ[2].
Энергетические эффекты растворения
Растворение может сопровождаться поглощением или выделением тепла:
- Эндотермическое растворение: поглощение тепла, температура раствора понижается. Растворимость таких веществ обычно увеличивается с повышением температуры.
- Экзотермическое растворение: выделение тепла, температура раствора повышается. Растворимость таких веществ может уменьшаться с повышением температуры[3].
Заключение
Понимание растворимости и факторов, на неё влияющих, важно для различных областей науки и техники. Знание о том, как изменяется растворимость в зависимости от условий, позволяет управлять процессами растворения и кристаллизации, что важно в химической промышленности, медицине и экологии.ё
Примечания
- ↑ Кузьменко Н. Е., Ерёмин В. В., Попков В. А. Начала химии. — М.: Лаборатория знаний, 2016. — 707 с.
- ↑ Физико-химические методы анализа. Дата обращения: 17 апреля 2025.
- ↑ Школьников Е. В. Термохимия растворов электролитов. — СПб.: Санкт-Петербургский государственный лесотехнический университет имени С. М. Кирова, 2022. — 32 с.
Литература
- Кузнецова Н. Е., Гара Н. Н., Титова И. М. Химия. 10 класс. Углубленный уровень. — 2019. — 409 с.
- Габриелян О. С., Остроумов И. Г., Пономарев С. Ю. Химия. 10 класс. Углубленный уровень. — "Российский учебник", 2019. — 364 с.
- Еремин В. В., Кузьменко Н. Е., Теренин В. И., Дроздов А. А., Лунин В. В. Химия. 10 класс. Углубленный уровень. — "Дрофа", 2019. — 409 с.
- Еремин В. В., Кузьменко Н. Е., Дроздов А. А., Лунин В. В. Химия. 11 класс. Углубленный уровень. — "Российский учебник", 2019. — 409 с.
- Габриелян О. С., Лысова Г. Г. Химия. 11 класс. Углубленный уровень. — "Дрофа", 2019. — 394 с.