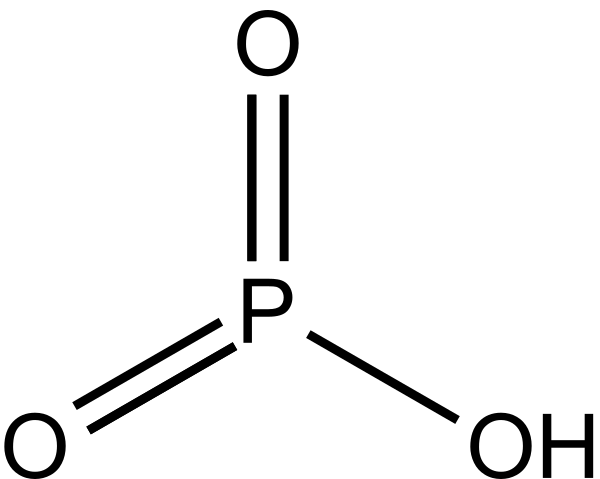
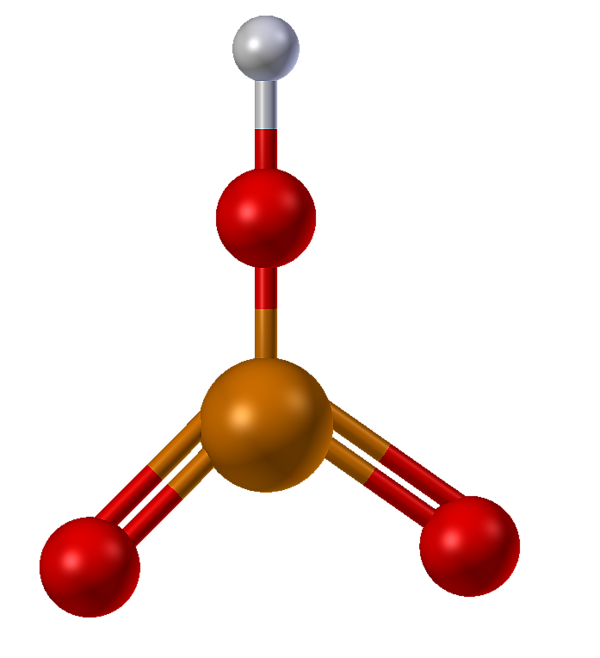
Метафосфорная кислота
Метафосфорная кислота — одноосновная кислота, простейшая формула которой HPO3; действительный же состав её молекул выражается формулой (HPO3)n, где n = 3,4,5 и т. д. В чистом виде представляет собой стекловидную массу, легко растворимую в воде. В раствор она переходит в виде полимера, который имеет кольцевую структуру. Через некоторое время кольца расщепляются и образуются полифосфорные кислоты с цепным строением молекул. Она очень ядовита. Однако соли метафосфорной кислоты (метафосфаты) применяют для смягчения воды, снижения её коррозионной активности, для удаления накипи с паровых котлов, кроме того, метафосфаты входят в состав некоторых моющих средств[1].
Общие сведения
| Метафосфорная кислота | |
|---|---|
| Общие | |
| Систематическое наименование |
Метафосфорная кислота |
| Хим. формула | (HPO3)n, n ≥ 3 |
| Классификация | |
| Рег. номер CAS | 37267-86-0 |
| 3D model (JSmol) | Интерактивная схема |
| PubChem | 3084658 |
| UNII | MTK99R3UV0 |
| CompTox Dashboard EPA | DTXSID40159485 |
| SMILES | |
| InChI | |
| ChemSpider | 495 |
| Безопасность | |
| Токсичность | Едкая кислота |
| Пиктограммы ECB |
|
| NFPA 704 | |
Получение
- Взаимодействие оксида фосфора(V) c водой на холоде[2]:
Качественная реакция
Качественной реакцией на метафосфорную кислоту может служить взаимодействие с нитратом серебра. Раствор кислоты помещают в пробирку, далее осторожно по стенке пробирки приливают водный раствор аммиака, а затем нитрат серебра. Аммиак необходим для нейтрализации образующейся азотной кислоты, потому что соль серебра может существовать только в слабощелочной или нейтральной среде.
Осадок имеет белый цвет.
Физико-химические свойства
Метафосфорная кислота представляет собой белое стеклообразное вещество, хорошо растворимое в воде и, присоединяя её, постепенно переходит в ортофосфорную кислоту:
См. также
Примечания
Литература
- Химическая энциклопедия / Редкол.: Кнунянц И.Л. и др.. — М.: Советская энциклопедия, 1992. — Т. 3. — 639 с. — ISBN 5-82270-039-8.
- Справочник химика / Редкол.: Никольский Б.П. и др.. — 2-е изд., испр. — М.—Л.: Химия, 1966. — Т. 1. — 1072 с.
- Справочник химика / Редкол.: Никольский Б.П. и др.. — 3-е изд., испр. — Л.: Химия, 1971. — Т. 2. — 1168 с.