Металлическая связь (ЕГЭ-ОГЭ)
Металлическая связь — это тип химической связи в металлическом кристалле, возникающий за счёт обобществления валентных электронов. Электроны валентной оболочки становятся общими для всего кристалла, формируя «электронный газ», который удерживает положительные ионы металла в узлах кристаллической решётки. Благодаря этой связи металлы характеризуются такими физическими свойствами, как прочность, пластичность, теплопроводность, электрическая проводимость, непрозрачность и блеск.
Основные понятия
- Электронный газ — совокупность свободно движущихся валентных электронов в металле, не принадлежащих отдельным атомам и обеспечивающих проводимость электрического тока и тепла.
- Положительные ионы — атомы металла, утратившие валентные электроны и образующие упорядоченную кристаллическую решётку.
- Кристаллическая решётка металла — регулярное пространственное расположение положительно заряженных ионов в твёрдом теле металла.
Механизм металлической связи
В металлических кристаллах валентные электроны становятся общими для всех атомов и свободно перемещаются среди положительных ионов, образуя «электронный газ». Электроны выполняют роль «связующего вещества», удерживая ионы между собой благодаря электростатическому притяжению и преодолевая отталкивание одноимённо заряженных частиц.
Положительные ионы металла занимают узлы кристаллической решётки. Между ними перемещаются электроны проводимости, высвобождённые из атомов при ионизации. В пределах решётки свободные электроны удерживаются ионами и не покидают её.
Кристаллические решётётки металлов
Большинство металлов образует плотные высокосимметричные кристаллические решётётки:
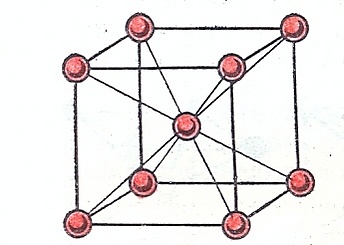
- Кубическая объёмноцентрированная (ОЦК) — атомы занимают позиции в вершинах и в центре куба. Примеры: литий (Li), натрий (Na), калий (K), железо (α-Fe).
- Кубическая гранецентрированная (ГЦК) — атомы расположены в вершинах куба и в центрах его граней. Примеры: медь (Cu), серебро (Ag), золото (Au), алюминий (Al).
- Гексагональная плотноупакованная (ГПУ) — атомы укладываются в слои с гексагональной симметрией. Примеры: магний (Mg), цинк (Zn), титан (α-Ti).
Свойства металлов, связанные с металлической связью
- Электропроводность — способность проводить электрический ток за счёт перемещения свободных электронов.
- Теплопроводность — передача тепла посредством переноса энергии электронным газом.
- Пластичность и ковкость — возможность деформироваться без разрушения благодаря делокализации металлической связи и подвижности ионов в решётке.
- Металлический блеск — отражение света на поверхности металла за счёт свободных электронов.
Расплавы металлов
В расплавленном состоянии металлы сохраняют металлическую связь. Свободные электроны продолжают удерживать положительные ионы вместе, что обеспечивает расплавам высокую электропроводность и теплопроводность. В качестве примера выступает ртуть, находящаяся в жидком виде при комнатной температуре и демонстрирующая типичные свойства металлов.
Заключение
Металлическая связь представляет собой специфический вид химической связи, присущий металлам и их сплавам. Именно она определяет такие уникальные физические свойства, как высокая электропроводность, значительная теплопроводность, пластичность и металлический блеск. Понимание механизма металлической связи имеет ключевое значение при разработке новых материалов и технологий, применяемых в науке и промышленности.