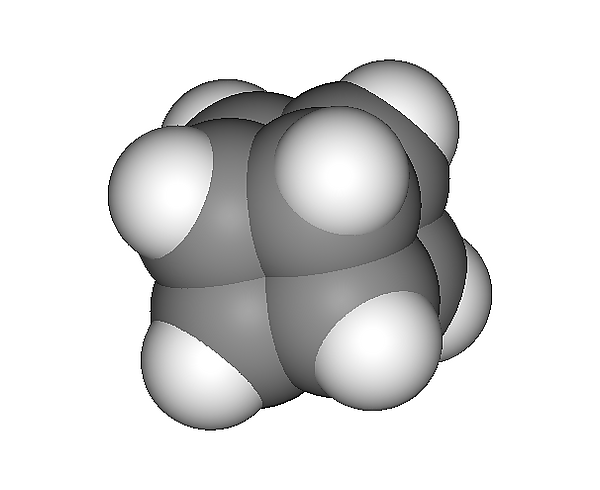
Кубан
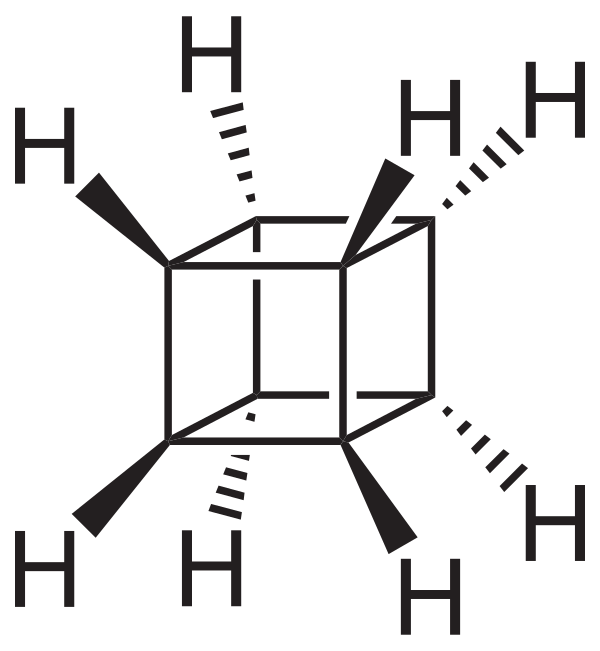
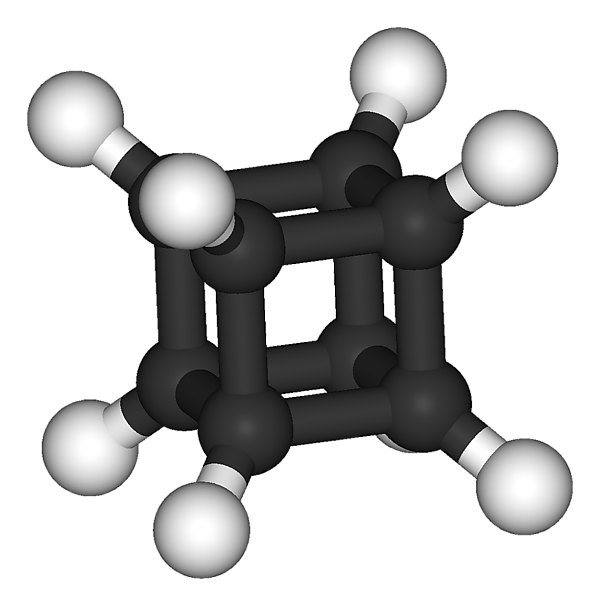
Кубан пентацикло[4.2.0.02,5.03,8.04,7]октан — химическое соединение с формулой C8H8, каркасный углеводород, атомы углерода которого расположены в пространстве в вершинах куба. Впервые получен в 1964 году Ф. Итоном, профессором химии Университет Чикаго[1]. Является одним из пяти «платоновых углеводородов», наряду с тетраэдраном, октаэдраном, додекаэдраном и икосаэдраном.
Индивидуальное вещество представляет собой белые кристаллы, хорошо растворимые в органических растворителях.
Вещество обладает очень высокой для углеводородов плотностью — 1,29 г/см³ . Производные кубана (например, октанитрокубан и гептанитрокубан) представляют собой плотные и высокоэффективные взрывчатые вещества.
Что важно знать
| Кубан | |
|---|---|
| Общие | |
| Систематическое наименование |
пентацикло[4.2.0.02,5.03,8.04,7]октан |
| Хим. формула | C8H8 |
| Физические свойства | |
| Молярная масса | 104,15 г/моль |
| Плотность | 1,29 г/см³ |
| Термические свойства | |
| Температура | |
| • плавления | 131 °C |
| • разложения | 200 |
| Классификация | |
| Рег. номер CAS | 277-10-1 |
| 3D model (JSmol) | Интерактивная схема |
| PubChem | 136090 |
| UNII | Z5HM0Q7DK1 |
| CompTox Dashboard EPA | DTXSID50182062 |
| SMILES | |
| InChI | |
| ChEBI | 33014 |
| ChemSpider | 119867 |
Получение
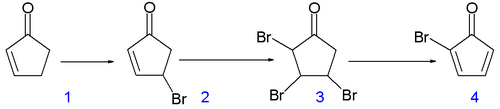
В качестве исходного соединения в оригинальном методе синтеза использован 2-циклопентенон.[2]:
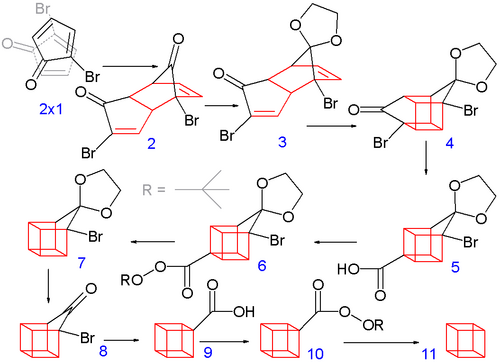
Аллильное бромирование прекурсора N-бромсукцинимидом по Циглеру в тетрахлоруглероде и последующее бромирование образующегося ненасыщенного соединения приводит к образованию 2,3,4-трибромпроизводного циклопентанона. Посредством элиминирования двух эквивалентов бромоводорода из полученного соединения в диэтиловом эфире в присутствии диэтиламина получают бромциклопентадиенон.
Последующая димеризация полученного соединения по реакции Дильса-Альдера протекает самопроизвольно и аналогична димеризации 1,3-циклопентадиена в бициклопентадиен. При этом стерическое отталкивание атомов брома и карбонильных групп благоприятствует формированию эндо-изомера в соответствии с правилом Альдера. Далее одну из кетогрупп стереоселективно защищают этиленгликолем в присутствии TsOH в бензоле и проводят фотохимическую внутримолекулярную реакцию [2+2]-циклоприсоединения. Галогенкетонную группировку далее переводят в карбоксилат-ион, используя для этой цели перегруппировку Фаворского, и проводят декарбоксилирование. Наконец, снятие кетальной защиты, повторная перегруппировка Фаворского и декарбоксилирование приводят к получению необходимого продукта.
Примечания