Валентные электроны (ЕГЭ-ОГЭ)
Валентные электроны — это те электроны, которые располагаются на самой внешней электронной оболочке атома. Именно они обуславливают химические свойства элемента и принимают участие в формировании химических связей при протекании химических реакций.
Основные понятия
- Валентная оболочка — последний заполненный электронный уровень атома, на котором находятся валентные электроны.
- Валентность — число связей, которые атом данного элемента может устанавливать с соседними атомами.
- Электронная конфигурация — распределение электронов атома по энергетическим уровням и соответствующим подуровням.
Количество валентных электронов
У элементов главных подгрупп число валентных электронов равно номеру их группы в периодической системе Менделеева (за исключением переходных металлов):
| Группа | Число валентных электронов |
|---|---|
| Группа 1 (щелочные металлы) | 1 |
| Группа 2 (щёлочноземельные металлы) | 2 |
| Группа 13 (подгруппа бора) | 3 |
| Группа 14 (подгруппа углерода) | 4 |
| Группа 15 (пниктогены) | 5 |
| Группа 16 (халькогены) | 6 |
| Группа 17 (галогены) | 7 |
| Группа 18 (инертные газы) | 8[1] |
Электронные конфигурации
Определение валентных электронов производится на основании электронной конфигурации атома. У элементов главных подгрупп валентные электроны располагаются на том энергетическом уровне, чей главный квантовый номер n максимален. Например, для фосфора (P) электронная конфигурация выглядит так:
- 1s2 2s2 2p6 3s2 3p3
У фосфора валентные электроны размещены на уровне n = 3 и составляют пять частиц (3s2 3p3).
Химические реакции
Валентные электроны участвуют в образовании химических связей:
- Атомы, у которых мало валентных электронов (1–3), обычно отдают их и превращаются в положительно заряженные ионы (катионы).
- Атомы с более значительным числом валентных электронов (5–7) стремятся либо присоединить дополнительные электроны, становясь отрицательными ионами (анионами), либо делить их с другими атомами, образуя ковалентные связи.
- Элементы с замкнутой валентной оболочкой (8 электронов) проявляют химическую инертность (инертные газы).
Так, натрий (Na) с одним валентным электроном охотно отдаёт его, образуя катион Na+. Хлор (Cl), располагая семью валентными электронами, склонен захватить ещё один, давая анион Cl−. При взаимодействии Na и Cl формируется ионная связь, приводящая к образованию NaCl.
Электропроводность
Валентные электроны оказывают влияние на проводимость материалов:
- Металлы обладают небольшим числом валентных электронов, которые свободно перемещаются, что обеспечивает их высокую электропроводность.
- Неметаллы характеризуются заполненной или почти завершённой валентной оболочкой, вследствие чего их электроны прочно связаны, делая эти элементы изоляторами.
- Полупроводники (например, кремний) демонстрируют промежуточные свойства: их проводимость варьируется в зависимости от условий и может меняться при легировании или изменении температуры.
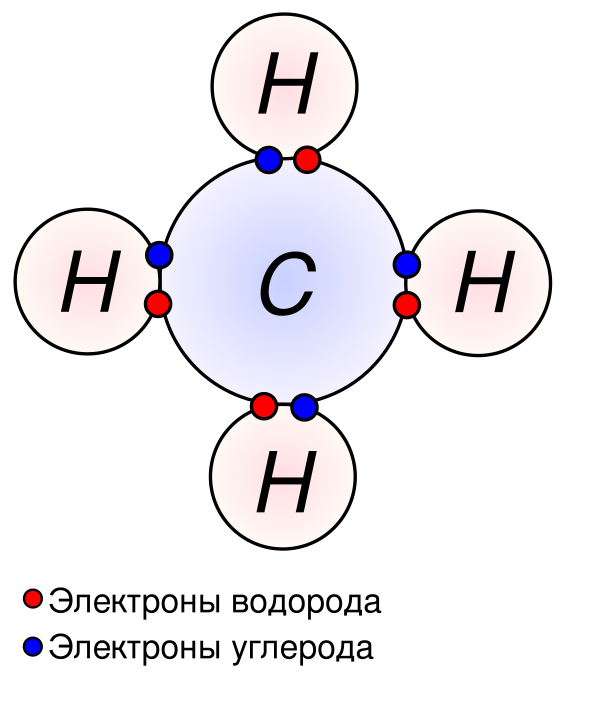
Пример ковалентной связи
Заключение
Валентные электроны имеют решающее значение для химических реакций и характеристик элементов. Знание их числа и расположения даёт возможность прогнозировать поведение атомов при взаимодействии, виды формируемых связей и свойства образующихся соединений.